
Барактын мазмунунун индекси
En Макул бассейн реформасы, ичинде бул бөлүмдө рН деңгээлиндеги бассейндер дарылайбыз бассейн суунун баалуулуктарындагы ph жана poh ортосундагы айырма.
Бассейндеги рН деген эмне жана анын деңгээли кандай болушу керек?

бассейндер үчүн идеалдуу рН эмнени билдирет (7,2-7,4)
рН кыскартуусу потенциалдуу суутекти билдирет жана суунун кычкылдуулугун же негиздүүлүгүн көрсөткөн өлчөм болуп саналат.
анда, рН суутектин потенциалын билдирет, бул көлөмдөгү суудагы суутек иондорунун концентрациясына туура келген маани, демек, суунун кычкылдыгын же негиздүүлүгүн көрсөткөн коэффициент. Демек, рН суудагы H+ иондорунун концентрациясын көрсөтүү, анын кислоталык же негизги мүнөзүн аныктоо үчүн жооптуу.
Бассейн суунун рН баалуулуктарынын шкаласы


Бассейн суусунун рН өлчөө шкаласы кандай баалуулуктарды камтыйт?
- рН өлчөө шкаласы 0дөн 14кө чейинки маанилерди камтыйт.
- Айрыкча 0 эң кислота, 14 эң негизги жана Нейтралдуу рН 7ге жайгаштырылат.
- Бул өлчөө заттагы эркин суутек иондорунун (Н+) саны менен аныкталат.

Эмне үчүн бизге рН керек?
рН суулуу эритменин кычкылдуулугун же негиздүүлүгүн аныктоо үчүн колдонулат. Суудагы эритменин кислота же негиз катары реакцияга кириши анын курамында суутек иондорунун (Н+) болушуна жараша болот.
Бирок, химиялык жактан таза жана нейтралдуу суу да суунун өз алдынча диссоциациялануусунан улам бир аз суутек иондорун камтыйт.
Белгилүү болгондой, тең салмактуулукта стандарттык шарттарда (750 мм рт.ст. жана 25°С) 1 л таза суунун курамында мең
y
мең
иондор, ошондуктан стандарттык температурада жана басымда (STP) суунун рН 7 болот.
Биздин бассейндин рН жөнгө салынбаганда эмне кылуу керек

Жогорку рН бассейнинин кесепеттерин жана бассейниңиздеги жогорку рНнын себептерин билиңиз

Бассейндин рН деңгээлин кантип көтөрүү керек жана ал төмөн болсо эмне болот

Жогорку же щелочтуу бассейндин pH деңгээлин кантип төмөндөтсө болот
рНдан тышкары бассейнди тейлөө боюнча көрсөтмөлөр: сууну тазалоо жана дезинфекциялоо

Бассейнди кантип тазалоону билүү үчүн пайдалуу колдонмо

Суу менен бассейнди кемчиликсиз абалда кармоо боюнча көрсөтмө
Кислоталык, нейтралдуу жана щелочтук рН көрсөткүчтөрү
рН баалуулуктарынын шкаласынын классификациясы
рН баалуулуктары кандай

рН шкаласы 1ден 14кө чейин барат, рН 7 нейтралдуу чечим болуп саналат.
Ошентип, рН логарифмдик шкалада 0 (өтө кислота) жана 14 (өтө щелоч) маанилеринин ортосунда туюнтулган маани болуп саналат; Ортодо биз 7 маанисин нейтралдуу катары табабыз.
рН масштабдуу универсалдуу рН көрсөткүчү
Заттын кислоталуу же щелочтук рН деңгээли бар деген эмнени билдирет?
Кислоталар жана негиздер деген эмне?
Кислоталар жана негиздер - жаратылышта бар жана рН деңгээли, башкача айтканда, кычкыл же щелочтук даражасы менен айырмаланган заттар. Заттардын кычкыл же щелоч экендигин аныктоо рН шкаласы аркылуу өлчөнгөн кычкылдуулуктун же щелочтуулуктун даражасы менен жөнгө салынат жана 0дөн (өтө кычкылдык 14кө чейин (өтө щелоч) диапазондо болот. Бирок экөө тең көбүнчө жегич, көбүнчө уулуу заттар болуп саналат. ошентсе да, көптөгөн өнөр жай жана адам колдонмолору бар.
Кислоталуу заттар деген эмне?
- Кислота рН деңгээли: рН 7ден аз
рН мааниси кислоталуу деген эмнени билдирет?
- Заттын кислоталуу болушу анын H-ге бай экенин билдирет+ (Суутек иондору): рН 7ден жогору
- Демек, Кислоталар - рН 7ден төмөн болгон заттар. (суунун рН 7ге барабар, нейтралдуу деп эсептелет), анын химиясында сууну кошкондо көбүнчө суутек иондору көп болот. Алар, адатта, протондорду жоготуу менен башка заттар менен реакцияга кирет (H+).
Нейтралдуу заттар деген эмне?
- Нейтралдуу рН мааниси: pH 7-ге барабар
рН мааниси нейтралдуу деген эмнени билдирет?
- рН суунун канчалык кислоталуу/негиздик экендигинин өлчөмү.
- Диапазон 0дөн 14кө чейин, 7 нейтралдуу.
щелочтуу заттар деген эмне?
- Негиздик же щелочтук рН менен заттар: рН 7ден жогору.
рН мааниси щелочтуу болгондо эмнени билдирет?
- Заттын щелочтуу болушу анын Н-ге начар экенин билдирет+ (же OH негиздерине бай-, H нейтралдаштырат+).
- Ушунун бардыгы үчүн, Негиздер, экинчи жагынан, рН 7ден жогору болгон заттар., алар суулуу эритмелерде көбүнчө гидроксил иондорун (OH-) ортосунда. Алар күчтүү кычкылдантуучу болуп саналат, башкача айтканда, курчап турган чөйрөнүн протондору менен реакцияга кирет.
рН жана pOH маанилеринин ортосундагы айырмачылыктар

Алар кандайча байланыштуу жана ph жана poh өлчөөлөрүнүн ортосунда кандай айырмачылыктар бар?
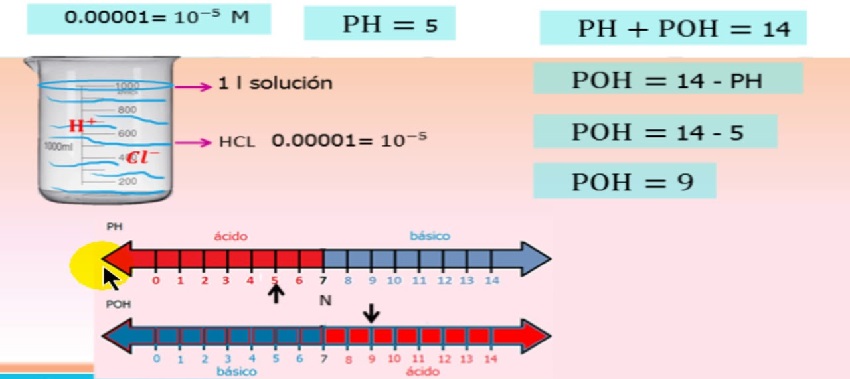
Албетте, иондордун активдүүлүгү ион концентрациясынан көз каранды жана бул теңдемеде сүрөттөлгөн
pH/poH ион активдүүлүгүнүн теңдемеси
кайда, – суутек ионунун активдүүлүгү
– суутек ионунун активдүүлүк коэффициенти
– суутек ионунун концентрациясы
Активдүүлүк коэффициенти ион концентрациясынын функциясы жана эритме барган сайын суюлганда 1ге жакындайт.
Суюлтулган (идеалдуу) эритмелер үчүн эриген заттын стандарттык абалы 1,00 М, ошондуктан анын молярдуулугу анын активдүүлүгүнө барабар.
Ошентип, идеалдуу чечимдерди кабыл алган маселелердин көбү үчүн активдүүлүк эмес, молярдык концентрациянын 10-базасынын логарифмасын колдонсок болот.
рН жана pOH маанисинин ортосундагы айырмачылыктар

нормалдуу рН мааниси кандай?
- Башкача айтканда, рН бул өлчөө болуп саналат эритменин кислоталык же щелочтуулугун аныктоо үчүн колдонулат. "p" "потенциал" дегенди билдирет, ошондуктан рН: суутек потенциалы деп аталат.
pOH мааниси кандай?
- Сиздин тарапыңыз үчүн. pOH - эритмедеги гидроксил иондорунун концентрациясынын өлчөмү. Ал гидроксил ионунун концентрациясынын 10 терс логарифминин негизи катары көрсөтүлөт жана рНдан айырмаланып, эритменин щелочтук деңгээлин өлчөө үчүн колдонулат.

рН же pOH мааниси кантип эсептелет?
ph шкаласынын маанилеринин формуласы кандай?
- Белгилүү болгондой, илимий чөйрөдө, pH чара болуп саналат de ичиндеги иондор de чечим. Сиз керек болушу мүмкүн рН эсептөө топтолууга негизделген. Эсептеңиз pH теңдемесин колдонуу pH: pH = -log[H3O+].
pOH эсептөө үчүн формула кандай?
- Мындан тышкары, pOH (же OH потенциалы) эритменин негиздүүлүгүнүн же щелочтуулугунун өлчөмү. Ошондой эле se pH = – log [H3O+] гидроний иондорунун концентрациясын өлчөө үчүн [Н3O+].

рН же pOH маанисин эсептөө үчүн негизги теңдеме
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [ой-] = 10-pOH
- pH + pOH =pKw = 14.00 25 °C.
рН баалуулуктарынын шкаласы менен pOH шкаласынын ортосунда кандай айырма бар?
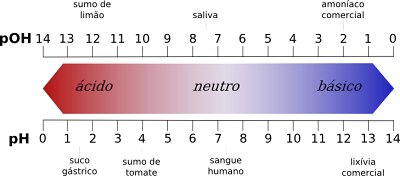
рН шкаласынын маанилеринин ортосундагы теңсиздик
- Бир жагынан алганда, рН шкаласы кислотанын 1ден 6га чейинки маанилерин берет, ал эми pOH шкаласы 8ден 14кө чейин кислотанын маанилерин берет.
- Тескерисинче, рН шкаласы 8ден 14кө чейин негизги маанилерди берет, ал эми pOH шкаласы 1ден 6га чейин негизги маанилерди берет.
ph жана pOH алардын маанилери менен логарифмдик масштабдагы байланышы
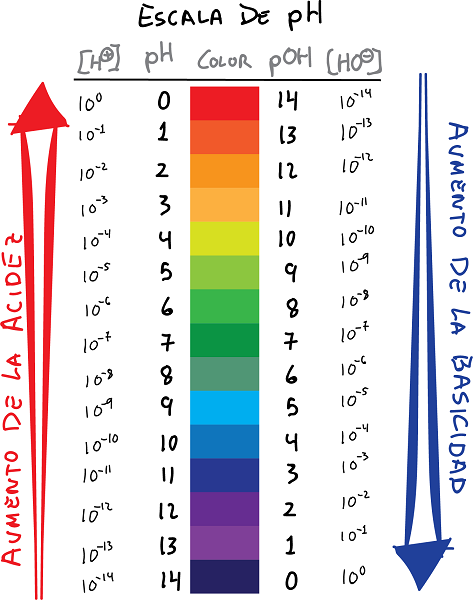
түстөр жана баалуулуктар менен ph жана pOH шкала байланышы
- pH Н иондорунун концентрациясынын логарифми болуп саналат+, белгиси өзгөргөн:
- Ошо сыяктуу эле, аныктоо pOH OH ионунун концентрациясынын логарифм катары-, белгиси өзгөргөн менен: ортосунда төмөнкүдөй байланыш түзүлүшү мүмкүн pH жана pOH.
- Негизинен, рН маанилери суутек ионунун концентрациясынын терс логарифмин берет, ал эми pOH мааниси гидроксид ионунун концентрациясынын терс логарифмин берет.
рН жана pOH маанилеринин масштабынын ортосундагы айырма
ph маанисинин таблицасы менен pOH маанисинин ортосундагы келишпестиктер
Андан кийин, биз сизге тасманы сунуштайбыз, анда рН суутек иондорунун концентрациясын, ал эми pOH гидроксил аниондорунун же гидроксид иондорунун концентрацияларын өлчөй турганын көрө аласыз.


