
Էջի բովանդակության ինդեքս
En Ok Pool Reform, այս բաժնում շրջանակներում pH մակարդակի լողավազաններ մենք կբուժենք ph-ի և poh-ի միջև տարբերությունը լողավազանի ջրի արժեքներում:
Որքա՞ն է pH-ն լողավազանում և ինչպիսի՞ն պետք է լինի դրա մակարդակը:

Ի՞նչ է նշանակում իդեալական pH լողավազանների համար (7,2-7,4)
pH հապավումը նշանակում է պոտենցիալ ջրածին և չափիչ է, որը ցույց է տալիս ջրի թթվայնությունը կամ հիմնայինությունը:
Հետո, pH-ը վերաբերում է ջրածնի պոտենցիալին, մի արժեք, որը համապատասխանում է ջրածնի իոնների կոնցենտրացիային ձեր ավազանի ջրում և, հետևաբար, այն գործակիցն է, որը ցույց է տալիս ջրի թթվայնության կամ հիմնայինության աստիճանը: Հետևաբար, pH-ը պատասխանատու է ջրի մեջ H+ իոնների կոնցենտրացիան ցույց տալու համար՝ որոշելով դրա թթվային կամ հիմնային բնույթը։
Լողավազանի ջրի pH արժեքների սանդղակ


Ի՞նչ արժեքներ է ներառում լողավազանի ջրի pH-ի չափման սանդղակը:
- pH-ի չափման սանդղակը ներառում է արժեքներ 0-ից 14:
- Հատկապես լինելով 0 ամենաթթվային, 14-ը՝ ամենահիմնականը և չեզոք pH-ը դնելով 7-ի վրա:
- Այս չափումը որոշվում է նյութում առկա ազատ ջրածնի իոնների (H+) քանակով։

Ինչու՞ մեզ պետք է pH:
pH-ը չափիչ է, որն օգտագործվում է ջրային լուծույթի թթվայնությունը կամ հիմնայինությունը որոշելու համար: Ջրային լուծույթը արձագանքում է որպես թթու կամ հիմք, կախված է ջրածնի իոնների (H+) պարունակությունից:
Այնուամենայնիվ, նույնիսկ քիմիապես մաքուր և չեզոք ջուրը պարունակում է որոշ ջրածնի իոններ ջրի ինքնատարանջատման պատճառով:
Հայտնի է, որ ստանդարտ պայմաններում (750 մմ Hg և 25°C) հավասարակշռության դեպքում 1 լ մաքուր ջուրը պարունակում է. մոլ
y
մոլ
իոններ, հետևաբար, ջուրը ստանդարտ ջերմաստիճանի և ճնշման (STP) ունի pH 7:
Ինչ անել, երբ մեր լողավազանի pH-ն ՉԻ կարգավորվում

Ինչպես բարձրացնել լողավազանի pH-ը և ինչ է տեղի ունենում, եթե այն ցածր է

Ինչպես իջեցնել բարձր կամ ալկալային ավազանի pH-ը

Լողավազանի pH-ի բարձրացման 5 արդյունավետ մեթոդ
Ուղեցույցներ, թե ինչպես կատարել լողավազանների սպասարկում pH-ից բացի՝ ջրի մաքրում և ախտահանում

Օգտակար ուղեցույց՝ իմանալու համար, թե ինչպես մաքրել լողավազանը

Ջրով լողավազան կատարյալ վիճակում պահելու ուղեցույց
Թթվային, չեզոք և ալկալային pH արժեքներ
pH արժեքների սանդղակի դասակարգում
Որոնք են pH արժեքները

pH սանդղակը գնում է 1-ից 14, իսկ pH 7-ը չեզոք լուծույթ է:
Այսպիսով, պարզվում է, որ pH-ն արժեք է, որն արտահայտվում է լոգարիթմական մասշտաբով 0 (չափազանց թթվային) և 14 (չափազանց ալկալային) արժեքների միջև. Միջանկյալ հատվածում մենք գտնում ենք, որ 7 արժեքը կատալոգավորված է որպես չեզոք:
pH սանդղակի ունիվերսալ pH ցուցիչ
Ի՞նչ է նշանակում, որ նյութն ունի թթվային կամ ալկալային pH մակարդակ:
Որոնք են թթուները և հիմքերը:
Թթուները և հիմքերը բնության մեջ գոյություն ունեցող նյութեր են և տարբերվում են իրենց pH մակարդակով, այսինքն՝ թթվայնության կամ ալկալայնության աստիճանով։ Նյութերի թթվային կամ ալկալային լինելու որոշումը որոշվում է թթվայնության կամ ալկալայնության աստիճանով, որը չափվում է pH սանդղակի միջոցով և տատանվում է 0-ից (չափազանց թթվային մինչև 14 (չափազանց ալկալային): Այնուամենայնիվ, երկուսն էլ սովորաբար քայքայիչ, հաճախ թունավոր նյութեր են, որոնք: Այնուամենայնիվ, ունեն բազմաթիվ արդյունաբերական և մարդկային կիրառություններ:
Որոնք են թթվային նյութերը:
- Թթվային pH մակարդակը՝ pH 7-ից պակաս
Ի՞նչ է նշանակում, որ pH արժեքը թթվային է:
- Որ նյութը թթվային է, նշանակում է, որ այն հարուստ է Հ+ (ջրածնի իոններ): 7-ից ավելի pH
- Հետևաբար, Թթուները 7-ից պակաս pH ունեցող նյութեր են: (ջրի pH հավասար է 7-ի, համարվում է չեզոք), որի քիմիան սովորաբար պարունակում է մեծ քանակությամբ ջրածնի իոններ ջուր ավելացնելիս: Նրանք սովորաբար արձագանքում են այլ նյութերի հետ՝ կորցնելով պրոտոններ (H+).
Որո՞նք են չեզոք նյութերը:
- Չեզոք pH արժեքը՝ pH հավասար է 7-ի
Ի՞նչ է նշանակում, որ pH արժեքը չեզոք է:
- pH-ը չափում է, թե որքան թթվային/հիմնական է ջուրը:
- Շրջանակը 0-ից 14 է, 7-ը չեզոք է:
Որո՞նք են ալկալային նյութերը:
- Հիմնական կամ ալկալային pH ունեցող նյութեր՝ 7-ից մեծ pH.
Ի՞նչ է նշանակում, երբ pH-ի արժեքը ալկալային է:
- Որ նյութը ալկալային է, նշանակում է, որ այն աղքատ է Հ+ (կամ հարուստ OH հիմքերով-, որոնք չեզոքացնում են Հ+).
- Այս ամենի համար Մյուս կողմից, հիմքերը 7-ից մեծ pH ունեցող նյութեր են:, որոնք ջրային լուծույթներում սովորաբար ապահովում են հիդրօքսիլ իոններ (OH-) մեջտեղում. Նրանք հակված են լինել հզոր օքսիդանտներ, այսինքն՝ արձագանքում են շրջակա միջավայրի պրոտոններին։
Տարբերությունները pH և pOH արժեքների միջև

Ինչպե՞ս են դրանք կապված և որո՞նք են տարբերությունները ph և poh չափումների միջև:
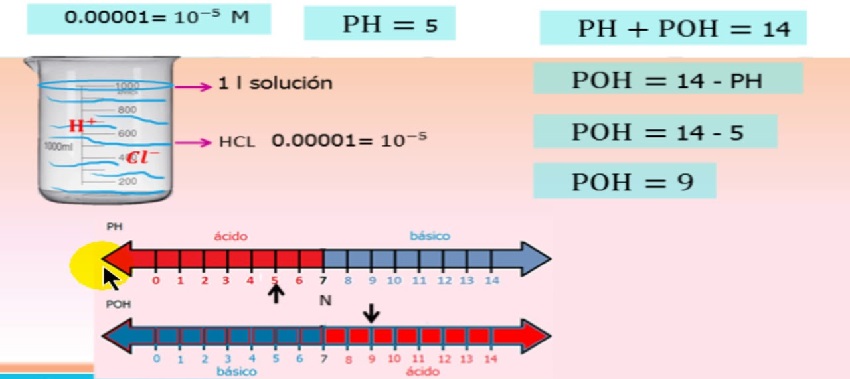
Իհարկե, իոնների ակտիվությունը կախված է իոնների կոնցենտրացիայից և դա նկարագրված է հավասարման մեջ
pH/poH իոնային ակտիվության հավասարումը
որտեղ, - ջրածնի իոնների ակտիվություն
- ջրածնի իոնի ակտիվության գործակիցը
- ջրածնի իոնի կոնցենտրացիան
Ակտիվության գործակիցը իոնների կոնցենտրացիայի ֆունկցիա է և մոտենում է 1-ին, քանի որ լուծույթն ավելի ու ավելի նոսրանում է:
Նոսրած (իդեալական) լուծույթների համար լուծված նյութի ստանդարտ վիճակը 1,00 Մ է, ուստի նրա մոլարությունը հավասար է ակտիվությանը:
Այսպիսով, խնդիրների մեծ մասի համար, որոնք ենթադրում են իդեալական լուծումներ, մենք կարող ենք օգտագործել լոգարիթմը մոլային կոնցենտրացիայի 10-րդ հիմքի համար, այլ ոչ թե ակտիվության:
Տարբերությունները pH-ի և pOH-ի արժեքի միջև

Ո՞րն է նորմալ pH արժեքը:
- Ինչ-որ կերպ, pH-ն այն չափումն է, որը օգտագործվում է լուծույթի թթվայնության կամ ալկալայնության մակարդակը որոշելու համար. «P»-ը նշանակում է «պոտենցիալ», այդ իսկ պատճառով pH-ը կոչվում է՝ ջրածնի պոտենցիալ:
Ո՞րն է pOH արժեքը:
- Ձեր կողմից: pOH-ը լուծույթում հիդրօքսիլ իոնների կոնցենտրացիայի չափումն է. Այն արտահայտվում է որպես հիդրօքսիլ իոնի կոնցենտրացիայի հիմնական 10 բացասական լոգարիթմ և, ի տարբերություն pH-ի, օգտագործվում է լուծույթի ալկալայնության մակարդակը չափելու համար։

Ինչպե՞ս է հաշվարկվում pH կամ pOH արժեքը:
Ո՞րն է ph սանդղակի արժեքների բանաձևը:
- Ինչպես արդեն հայտնի է, գիտական ոլորտում ի pH չափն է de իոնները ներսում de լուծում. Դուք կարող եք ստիպված լինել հաշվարկել pH կենտրոնացվածության վրա հիմնված. Հաշվեք pH Օգտագործելով հավասարումը pH: pH = -log[H3O+]:
Ո՞րն է pOH-ը հաշվարկելու բանաձևը:
- Նաեւ, pOH (կամ OH պոտենցիալ) լուծույթի հիմնականության կամ ալկալայնության չափում է: Նաև se օգտագործում է pH = – log [H3O+] հիդրոնիումի իոնների կոնցենտրացիան չափելու համար [H3O+].

Հիմնական հավասարումներ pH կամ pOH արժեքը հաշվարկելու համար
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [Օհ-] = 10-pOH
- pH + pOH =pKw = 14.00 25 °C-ում:
Ո՞րն է տարբերությունը pH արժեքների և pOH-ի սանդղակի միջև:
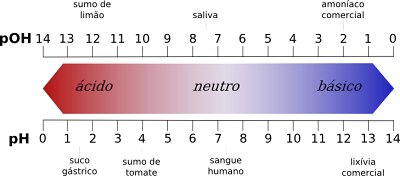
Անհավասարություններ pH սանդղակի արժեքների միջև
- Մի կողմից, pH սանդղակը տալիս է թթվային արժեքներ 1-ից 6, մինչդեռ pOH սանդղակը տալիս է թթվային արժեքներ 8-ից 14:
- Ընդհակառակը, pH սանդղակը տալիս է հիմնական արժեքներ 8-ից 14, մինչդեռ pOH սանդղակը տալիս է հիմնական արժեքներ 1-ից 6-ը:
ph-ի և pOH-ի լոգարիթմական սանդղակի հարաբերությունը նրանց արժեքների հետ
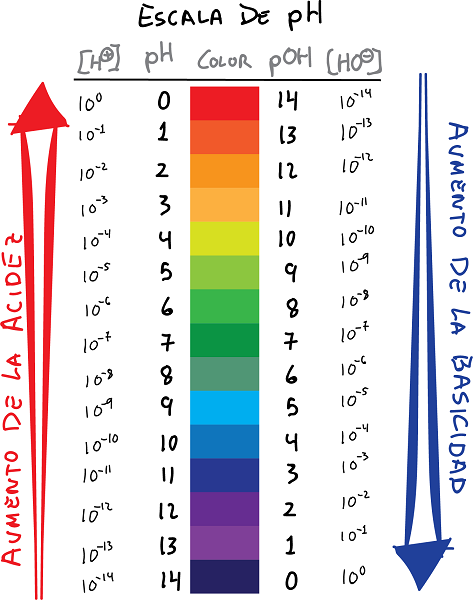
ph և pOH սանդղակի կապ գույների և արժեքների հետ
- pH H իոնների կոնցենտրացիայի լոգարիթմն է+, նշանը փոխված է.
- Նմանապես, սահմանեք pOH որպես OH իոնի կոնցենտրացիայի լոգարիթմ-, նշանը փոխված է pH y El pOH.
- Հիմնականում pH արժեքները տալիս են ջրածնի իոնի կոնցենտրացիայի բացասական լոգարիթմը, մինչդեռ pOH արժեքը տալիս է հիդրօքսիդի իոնի կոնցենտրացիայի բացասական լոգարիթմը:
Տարբերությունը pH-ի և pOH արժեքների սանդղակի միջև
Անհամապատասխանություններ ph արժեքի աղյուսակի և pOH արժեքի միջև
Դրանից հետո մենք ձեզ տրամադրում ենք ֆիլմ, որտեղ կարող եք տեսնել, որ pH-ը չափում է ջրածնի իոնների կոնցենտրացիաները, մինչդեռ pOH-ը չափում է հիդրօքսիլ անիոնների կամ հիդրօքսիդի իոնների կոնցենտրացիաները:


