
Innéacs ábhar an leathanaigh
En Ceart go leor Athchóiriú Snámha, san alt seo laistigh den linnte snámha leibhéal pH déileálfaimid leis an difríocht idir ph agus poh i luachanna uisce linne.
Cad é an pH i linn snámha agus conas ba cheart a leibhéil a bheith?

Cad a chiallaíonn pH idéalach do linnte snámha (7,2-7,4)
Seasann an t-acrainm pH do hidrigin ionchasach agus is tomhas é a léiríonn aigéadacht nó bunúsacht uisce.
Ansin, Tagraíonn pH don phoitéinseal hidrigine, luach a fhreagraíonn do thiúchan na n-ian hidrigine san uisce i do linn agus mar sin is é an chomhéifeacht a léiríonn leibhéal aigéadachta nó bunúsacht an uisce. Mar sin, tá an pH i gceannas ar thiúchan na n-ian H+ san uisce a léiriú, ag cinneadh a charachtar aigéadach nó bunúsach.
Scála luachanna pH uisce linn snámha


Cad iad na luachanna a chuimsíonn scála tomhais pH an uisce linne?
- Áirítear ar an scála tomhais pH luachanna ó 0 go 14.
- Go háirithe 0 an ceann is aigéadaí, 14 an ceann is bunúsaí agus an pH Neodrach ag 7.
- Cinntear an tomhas seo ag líon na n-ian saor hidrigine (H+) sa tsubstaint.

Cén fáth a bhfuil pH de dhíth orainn?
Is tomhas é pH a úsáidtear chun aigéadacht nó bunúsacht tuaslagáin uiscí a shonrú. Braitheann cibé an n-imoibríonn tuaslagán uiscí mar aigéad nó mar bhun ar a ábhar iain hidrigine (H+).
Mar sin féin, tá roinnt iain hidrigine ann fiú in uisce atá íon agus neodrach go ceimiceach mar gheall ar fhéin-dhíthiomsú uisce.
Tá sé ar eolas go bhfuil 750 L d'uisce íon i gcothromaíocht faoi choinníollacha caighdeánacha (25 mmHg agus 1 °C). caochÚn
y
caochÚn
iain, mar sin, tá pH 7 ag uisce ag teocht agus brú caighdeánach (STP).
Cad atá le déanamh nuair NACH bhfuil pH ár linne rialaithe

Bíodh a fhios agat na hiarmhairtí linne le pH ard agus na cúiseanna atá le pH ard i do linn

Conas pH na linne a ardú agus cad a tharlaíonn má tá sé íseal

Conas pH Ard nó Linn Alcaileach a ísliú
Treoracha maidir le conas cothabháil linnte a dhéanamh chomh maith le pH: glanadh uisce agus díghalrú

Treoir úsáideach le fios conas linn snámha a ghlanadh

Treoir maidir le linn snámha le huisce a chothabháil i riocht foirfe
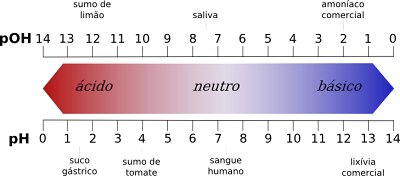
Luachanna pH aigéadacha, neodracha agus alcaileacha
Aicmiú Scála na Luachanna pH
Cad iad na luachanna pH?

Téann an scála pH ó 1 go 14, agus pH 7 ina réiteach neodrach.
Mar sin, tharlaíonn sé gur luach é pH a shloinntear ar scála logartamach idir na luachanna 0 (thar a bheith aigéadach) agus 14 (thar a bheith alcaileach); Idir an dá linn feicimid go bhfuil an luach 7 catalógaithe mar luach neodrach.
scála pH táscaire pH uilíoch
Cad a chiallaíonn sé go bhfuil leibhéal pH aigéadach nó alcaileach ag substaint?
Cad is aigéid agus bunanna ann?
Is substaintí iad aigéid agus bunanna atá sa nádúr agus a ndéantar idirdhealú orthu ag a leibhéal pH, is é sin, a leibhéal aigéadachta nó alcaileacht. Tá cinneadh an bhfuil substaintí aigéadach nó alcaileach á rialú ag an leibhéal aigéadachta nó alcaileachta arna thomhas tríd an scála pH agus raonta ó 0 (thar a bheith aigéadach go 14 (thar a bheith alcaileach). mar sin féin tá go leor feidhmeanna tionsclaíochta agus daonna acu.
Cad is substaintí aigéadacha ann?
- Leibhéal pH aigéad: pH níos lú ná 7
Cad a chiallaíonn sé go bhfuil an luach pH aigéadach?
- Ciallaíonn go bhfuil substaint aigéadach go bhfuil sé saibhir i H+ (iain hidrigine): pH níos mó ná 7
- Uaidh sin, Is substaintí iad aigéid a bhfuil pH níos lú ná 7 acu. (pH uisce cothrom le 7, meastar a bheith neodrach), a mbíonn méideanna móra iain hidrigine sa cheimic de ghnáth agus uisce á chur leis. De ghnáth imoibríonn siad le substaintí eile trí phrótóin a chailleadh (H+).
Cad is substaintí neodracha ann?
- Luach neodrach pH: pH cothrom le 7-
Cad a chiallaíonn sé go bhfuil an luach pH neodrach?
- Is tomhas é pH ar cé chomh aigéadach/bunúsach atá an t-uisce.
- Tá an raon ó 0 go 14, agus tá 7 neodrach.
Cad iad substaintí alcaileach?
- Substaintí a bhfuil pH bonn nó alcaileach acu: pH níos mó ná 7.
Cad a chiallaíonn sé go bhfuil an luach pH alcaileach?
- Ciallaíonn go bhfuil substaint alcaileach go bhfuil sé bocht i H+ (nó saibhir i mbonn OH-, a neodaíonn an H+).
- Chun seo go léir, Ar an láimh eile, is substaintí iad bunanna a bhfuil pH níos mó ná 7 acu., a sholáthraíonn iain hiodrocsaile (OH-) i lár. Is gnách gur ocsaídeoirí cumhachtacha iad, is é sin, imoibríonn siad le prótóin ón meán máguaird.
Difríochtaí idir luachanna pH agus pOH

Cén gaol atá leo agus cad iad na difríochtaí idir tomhais ph agus poh?
Ar ndóigh, braitheann gníomhaíocht na n-ian ar an tiúchan ian agus déantar cur síos air seo sa chothromóid
Cothromóid ghníomhaíocht ian pH/poH
áit, – gníomhaíocht ian hidrigine
– comhéifeacht gníomhaíochta an iain hidrigine
– tiúchan ian hidrigine
Feidhm de thiúchan ian is ea an chomhéifeacht ghníomhaíochta agus druideann sí le 1 de réir mar a éiríonn an tuaslagán níos caolaithe.
Maidir le tuaslagáin caol (idéalach), is é 1,00 M staid chaighdeánach an tuaslagáit, agus mar sin is ionann a mhólaracht agus a ghníomhaíocht.
Mar sin, don chuid is mó d’fhadhbanna a ghlacann le réitigh idéalacha is féidir linn an logarithm go dtí bonn 10 den tiúchan mólar a úsáid, ní an ghníomhaíocht.
Difríochtaí idir cad é luach pH agus pOH

Cad é an gnáthluach pH?
- Ar bhealach, is tomhas é pH a a úsáidtear chun leibhéal aigéadachta nó alcaileacht tuaslagáin a bhunú. Seasann an “p” do “acmhainneacht”, agus sin an fáth a dtugtar pH ar: poitéinseal hidrigine.
Cad é an luach pOH?
- Chun do chuid. Is tomhas é pOH de thiúchan na n-ian hiodrocsaile i dtuaslagán. Cuirtear in iúl é mar logarithm diúltach bonn 10 den tiúchan ian hiodrocsaile agus, murab ionann agus pH, úsáidtear é chun leibhéal alcaileachta tuaslagáin a thomhas.

Conas a ríomhtar an luach pH nó pOH?
Cad í an fhoirmle do luachanna scála ph?
- Mar is eol cheana féin, sa réimse eolaíoch, an pH Is é an beart de na hiain istigh de réiteach. Seans go mbeidh ort ríomh pH bunaithe ar thiúchan. Ríomh an pH Ag baint úsáide as cothromóid na pH: pH = -log[H3O+].
Cad í an fhoirmle chun pOH a ríomh?
- Chomh maith leis sin, an pOH (nó poitéinseal OH) tomhas ar bhunúsacht nó alcaileacht tuaslagáin. Chomh maith leis sin se úsáideann an pH = – log [H3O+] chun tiúchan na n-ian hidréine [H3O+].

Cothromóidí Buntábhachtacha chun an luach pH nó pOH a ríomh
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [ó-] = 10-pOH
- pH + pOH =pKw = 14.00 ag 25 °C.
Cad é an difríocht idir scála na luachanna pH agus scála pOH?
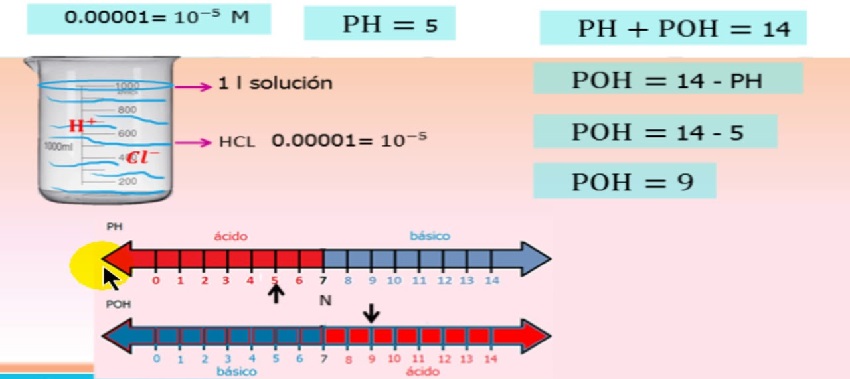
Éagothroime idir luachanna an scála pH
- Ar thaobh amháin, tugann an scála pH luachanna aigéid ó 1 go 6 agus tugann an scála pOH luachanna aigéid ó 8 go 14.
- Os a choinne sin, tugann an scála pH bunluachanna ó 8 go 14, agus tugann an scála pOH bunluachanna ó 1 go 6.
Coibhneas scála logartamach de ph agus pOH lena luachanna
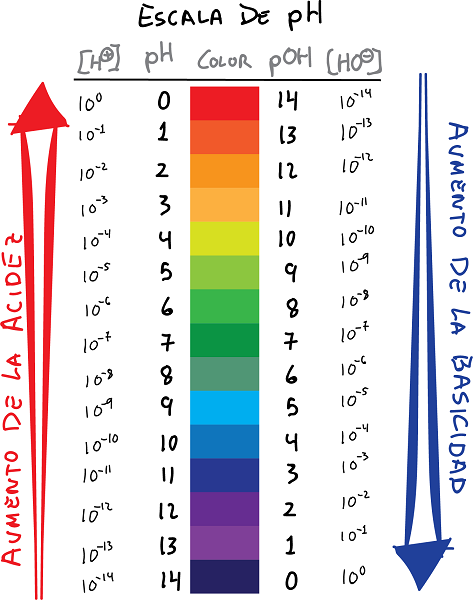
nasc scála ph agus pOH le dathanna agus luachanna
- pH is é logarithm thiúchan na n-ian H+, agus an comhartha athraithe:
- Mar an gcéanna, a shainiú pOH mar logarithm an tiúchan iain OH-, agus an comhartha athraithe: Is féidir an gaol seo a leanas a bhunú idir an pH agus pOH.
- Go bunúsach, tugann na luachanna pH logarithm diúltach an tiúchan ian hidrigine, agus tugann an luach pOH logarithm diúltach an tiúchan ian hiodrocsaíd.
Difríocht idir scála na luachanna pH agus pOH
Neamhréireachtaí idir an tábla luach ph agus luach pOH
Tar éis sin, cuirimid scannán ar fáil duit inar féidir leat a fheiceáil go dtomhaiseann pH tiúchain na n-ian hidrigine, agus tomhaiseann pOH tiúchain na n-ainian hiodrocsaile nó na n-ian hiodrocsaíde.


