
Inhoudsopgave van de pagina
En Ok zwembadhervorming, in deze sectie binnen de pH-waarde zwembaden we zullen de behandelen verschil tussen ph en poh in zwembadwaterwaarden.
Wat is de pH in een zwembad en hoe moeten de niveaus zijn?

Wat betekent de ideale pH voor zwembaden (7,2-7,4)
Het acroniem pH staat voor potentiële waterstof en is een maat die de zuurgraad of basiciteit van water aangeeft.
Vervolgens pH verwijst naar het potentieel van waterstof, een waarde die overeenkomt met de concentratie van waterstofionen in het water in uw zwembad en is daarom de coëfficiënt die de zuurgraad of basiciteit van het water aangeeft. Daarom is de pH verantwoordelijk voor het aangeven van de concentratie van H + -ionen in het water en bepaalt het zure of basische karakter ervan.
Schaal van pH-waarden van zwembadwater


Welke waarden bevat de pH-meetschaal van het zwembadwater?
- De pH-meetschaal bevat waarden van 0 tot 14.
- Met name 0 het meest zuur, 14 het meest basisch en de neutrale pH op 7.
- Deze meting wordt bepaald door het aantal vrije waterstofionen (H+) in de stof.

Waarom hebben we pH nodig?
pH is een maat die wordt gebruikt om de zuurgraad of basiciteit van een waterige oplossing te specificeren. Of een waterige oplossing als zuur of base reageert, hangt af van het gehalte aan waterstofionen (H+).
Zelfs chemisch zuiver en neutraal water bevat echter enkele waterstofionen als gevolg van zelfdissociatie van water.
Het is bekend dat bij evenwicht onder standaardomstandigheden (750 mmHg en 25°C) 1 L zuiver water mol
y
mol
ionen, daarom heeft water bij standaardtemperatuur en -druk (STP) een pH van 7.
Wat te doen als de pH van ons zwembad NIET gereguleerd is?

Hoe u de pH van het zwembad kunt verhogen en wat er gebeurt als deze laag is

Hoe een hoge of alkalische zwembad-pH te verlagen?

5 Effectieve methoden om de pH van het zwembad te verhogen
Gidsen voor het uitvoeren van zwembadonderhoud naast de pH: waterreiniging en desinfectie

Handige gids voor het schoonmaken van het zwembad

Gids voor het onderhoud van een zwembad met water in perfecte staat
Zure, neutrale en alkalische pH-waarden
Classificatie van de schaal van pH-waarden
Wat zijn de pH-waarden

De pH-schaal gaat van 1 tot 14, waarbij pH 7 een neutrale oplossing is.
Het blijkt dus dat pH een waarde is die wordt uitgedrukt op een logaritmische schaal tussen de waarden 0 (extreem zuur) en 14 (extreem alkalisch); Daartussen vinden we de waarde 7 gecatalogiseerd als neutraal.
pH-schaal universele pH-indicator
Wat betekent het dat een stof een zure of alkalische pH-waarde heeft?
Wat zijn zuren en basen?
Zuren en basen zijn stoffen die in de natuur voorkomen en zich onderscheiden door hun pH-waarde, dat wil zeggen door hun zuurgraad of alkaliteit. De bepaling of stoffen zuur of alkalisch zijn, wordt bepaald door de zuurgraad of alkaliteit gemeten via de pH-schaal en varieert van 0 (extreem zuur tot 14 (extreem alkalisch). Beide zijn echter meestal bijtend, vaak giftig, die hebben niettemin talrijke industriële en menselijke toepassingen.
Wat zijn zure stoffen?
- Zure pH-waarde: pH minder dan 7
Wat betekent het dat de pH-waarde zuur is?
- Dat een stof zuur is, betekent dat deze rijk is aan H+ (waterstofionen): pH hoger dan 7
- Vandaar, Zuren zijn stoffen met een pH lager dan 7. (pH van water gelijk aan 7, beschouwd als neutraal), waarvan de chemie gewoonlijk grote hoeveelheden waterstofionen bevat bij het toevoegen van water. Ze reageren meestal met andere stoffen door protonen te verliezen (H+).
Wat zijn neutrale stoffen?
- Neutrale pH-waarde: pH gelijk aan 7-
Wat betekent het dat de pH-waarde neutraal is?
- pH is een maat voor hoe zuur/basisch het water is.
- Het bereik is van 0 tot 14, waarbij 7 neutraal is.
Wat zijn alkalische stoffen?
- Stoffen met base of alkalisch pH: pH hoger dan 7.
Wat betekent het als de pH-waarde alkalisch is?
- Dat een stof alkalisch is, betekent dat deze arm is aan H+ (of rijk aan OH-basen-, die de H . neutraliseren+).
- Voor dit alles, Basen daarentegen zijn stoffen met een pH hoger dan 7., die in waterige oplossingen meestal hydroxylionen (OH-) middenin. Het zijn meestal krachtige oxidanten, dat wil zeggen, ze reageren met protonen uit het omringende medium.
Verschillen tussen pH- en pOH-waarden

Hoe zijn ze gerelateerd en wat zijn de verschillen tussen ph- en poh-metingen?
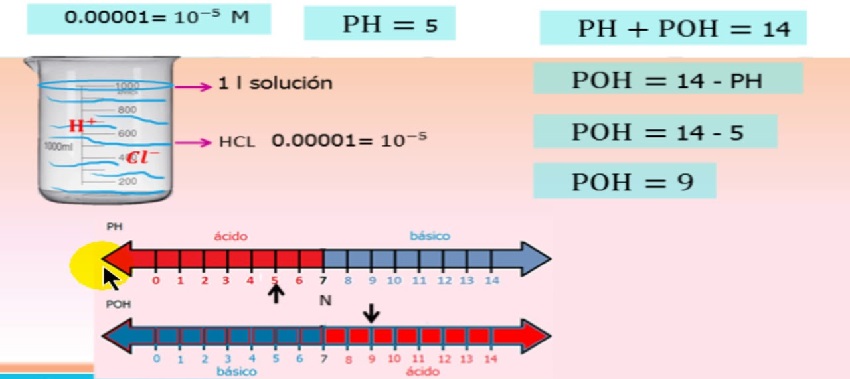
Natuurlijk hangt de activiteit van de ionen af van de ionenconcentratie en dit wordt beschreven in de vergelijking
pH/poH-ionactiviteitsvergelijking
waar, – waterstofionenactiviteit
– activiteitscoëfficiënt van het waterstofion
– waterstofionenconcentratie
De activiteitscoëfficiënt is een functie van de ionenconcentratie en benadert 1 naarmate de oplossing meer en meer verdund wordt.
Voor verdunde (ideale) oplossingen is de standaardtoestand van de opgeloste stof 1,00 M, dus de molariteit is gelijk aan de activiteit.
Dus voor de meeste problemen die ideale oplossingen veronderstellen, kunnen we de logaritme gebruiken tot het grondtal 10 van de molaire concentratie, niet de activiteit.
Verschillen tussen wat is de waarde van pH en pOH

Wat is de normale pH-waarde?
- In zekere zin is pH een maat die: gebruikt om de zuurgraad of alkaliteit van een oplossing vast te stellen. De "p" staat voor "potentieel", daarom wordt pH genoemd: potentieel van waterstof.
Wat is de pOH-waarde?
- Voor jouw deel. pOH is een maat voor de concentratie van hydroxylionen in een oplossing. Het wordt uitgedrukt als de negatieve logaritme van base 10 van de hydroxylionenconcentratie en wordt, in tegenstelling tot pH, gebruikt om het alkaliteitsniveau van een oplossing te meten.

Hoe wordt de pH- of pOH-waarde berekend?
Wat is de formule voor ph-schaalwaarden?
- Zoals al bekend is, in het wetenschappelijk veld, de pH is de maat? de de ionen binnen de een oplossing. Misschien moet je bereken pH gebaseerd op concentratie. Bereken de pH Met behulp van de vergelijking van pH: pH = -log[H3O+].
Wat is de formule om pOH te berekenen?
- Ook de pOH (of OH-potentiaal) is een maat voor de basiciteit of alkaliteit van een oplossing. Ook se gebruikt de pH = – log [H3O+] om de concentratie van hydroniumionen te meten [H3O+].

Belangrijkste vergelijkingen om de pH- of pOH-waarde te berekenen
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [oh-] = 10-pOH
- pH + pOH =p Kw = 14.00 bij 25 °C.
Wat is het verschil tussen de schaal van pH-waarden en die van pOH?
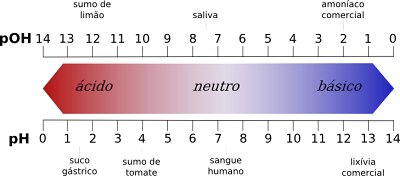
Ongelijkheden tussen de waarden van de pH-schaal
- Enerzijds geeft de pH-schaal zuurwaarden van 1 tot 6 terwijl de pOH-schaal zuurwaarden geeft van 8 tot 14.
- Omgekeerd geeft de pH-schaal basiswaarden van 8 tot 14, terwijl de pOH-schaal basiswaarden geeft van 1 tot 6.
Logaritme schaalrelatie van ph en pOH met hun waarden
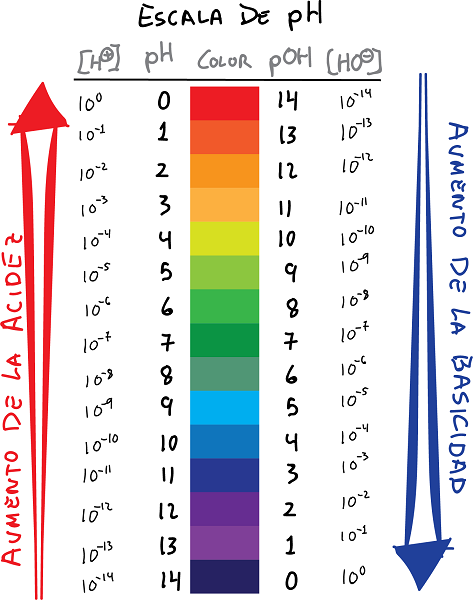
ph- en pOH-schaalverbinding met kleuren en waarden
- pH is de logaritme van de concentratie van H-ionen+, met het teken veranderd:
- Evenzo, definieer pOH als de logaritme van de OH-ionenconcentratie-, met het teken gewijzigd: De volgende relatie kan worden gelegd tussen de pH en pOH.
- Kortom, de pH-waarden geven de negatieve logaritme van de waterstofionenconcentratie, terwijl de pOH-waarde de negatieve logaritme van de hydroxide-ionenconcentratie geeft.
Verschil tussen de schaal van pH- en pOH-waarden
Verschillen tussen de ph-waardetabel en de pOH-waarde
Daarna geven we je een filmpje waarin je kunt zien dat pH de concentraties van waterstofionen meet, terwijl pOH de concentraties van hydroxylanionen of hydroxide-ionen meet.


