
පිටු අන්තර්ගතයේ දර්ශකය
En හරි සංචිත ප්රතිසංස්කරණය අපි ඔබ සමඟ ගනුදෙනු කරන පහත පළ කිරීම බෙදා ගැනීමට අවශ්යයි තටාකයේ pH අගය කුමක්ද සහ එය පාලනය කරන්නේ කෙසේද
pH යනු කුමක්ද, අගයන්, වැදගත්කම සහ එය මැනිය යුතු ආකාරය

PH අගය යනු කුමක්ද?
pH යනු ජලීය ද්රාවණයක ආම්ලිකතාවය හෝ ක්ෂාරීය බව මැනීමකි.
එබැවින්, අප දැන් කී පරිදි, PH යනු ඇතැම් ද්රාවණවල පවතින හයිඩ්රජන් අයන සාන්ද්රණය පෙන්නුම් කරන sutantica හි ආම්ලිකතාවය හෝ ක්ෂාරීයත්වය පිළිබඳ මිනුමක් වේ.
pH යන කෙටි යෙදුමෙන් අදහස් කරන්නේ කුමක්ද?
- අනෙක් අතට, එය සඳහන් කරන්න pH යන කෙටි යෙදුම හයිඩ්රජන් වල විභවය හෝ හයිඩ්රජන් අයන වල විභවය යන්නයි.
PH යනු කුමක්ද | මූලික රසායන විද්යාව
Ph අගයෙන් අදහස් කරන්නේ කුමක්ද යන්න පිළිබඳ පැහැදිලි කිරීමේ වීඩියෝව
මිනිස් සිරුරේ pH අගය සමතුලිත වීම
තටාකයේ pH මට්ටම

තටාකයේ ජලයේ pH අගය කුමක්ද?
තටාකයේ pH අගය කුමක්ද?

තටාකයේ pH අගයෙන් අදහස් කරන්නේ කුමක්ද?
එනම් තටාකයේ pH අගය
තටාකයේ pH අගය කුමක්ද: pH යනු හයිඩ්රජන් වල විභවය වන අතර එය ඔබගේ තටාකයේ ජලයේ ඇති හයිඩ්රජන් අයන සාන්ද්රණයට අනුරූප වන අගයක් වන අතර එහි ප්රතිඵලයක් ලෙස ජලයේ ආම්ලිකතාවයේ හෝ මූලිකත්වයේ මට්ටම පෙන්නුම් කරන සංගුණකය වේ. එමනිසා, pH අගය ජලයේ H+ අයන සාන්ද්රණය දැක්වීම, එහි ආම්ලික හෝ මූලික ස්වභාවය තීරණය කිරීම භාරව පවතී.
Ideal pool pH අගයන්
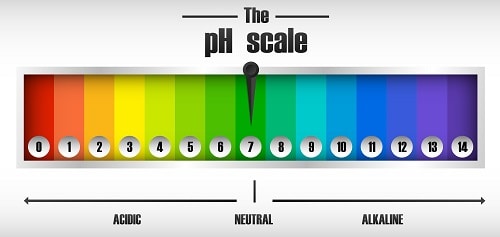
pH පරිමාණය 1 සිට 14 දක්වා වන අතර pH 7 උදාසීන විසඳුමක් වේ.
pH යනු 0 සහ 14 අගයන් අතර ලඝුගණක පරිමාණයකින් ප්රකාශිත අගයකි.
එබැවින්, ද්රවයක ආම්ලිකතාවය මැනීම සඳහා සහ අපගේ තටාකයේ ජලය, රසායනික ද්රව්ය සහ දැන් අපි භාවිතා කරමු pH පරිමාණය 0 සිට 14 දක්වා අගයන් ඇතුළත් වේ.
කදිම තටාක pH අගය
තටාකයේ pH අගය: තටාක නඩත්තු කිරීමේදී වඩාත් වැදගත් පරාමිතීන්ගෙන් එකකි.
තටාකයේ ජලය pH අගය සඳහා සුදුසු අගය: උදාසීන pH අගය 7.2 සහ 7.6 අතර පරමාදර්ශී පරාසය.

ඉතින් එතකොට, මෙම පරාසයේ pH අගය තිබීම ප්රශස්ත තත්ත්වයේ ජලය තිබීමට පමණක් හොඳ නොවේs අඩු හෝ ඉහළ pH අගය විෂබීජ නාශක බලපෑම සැලකිය යුතු ලෙස අඩු කරයි, නමුත් එය ද වේ ස්නානය කරන්නන්ගේ සම සහ ඇස් සඳහා වඩාත් සුදුසුය.
සේලයින් තටාකයේ pH අගය

ph සේලයින් තටාක
- ඇත්තටම, ද ph සේලයින් තටාකය නඩත්තු කිරීමේ සිට ක්ලෝරීන් සමඟ ප්රතිකාර කරන ලද තටාක වලට සමාන වේ තටාකය ලුණු භාවිතා කිරීම ද නිතිපතා නිරීක්ෂණය කිරීම අවශ්ය වේ pH ජලයේ.
- එබැවින් ලුණු තටාකවල pH අගය ද තිබිය යුතුය pH 7 සහ 7,6 අතර පිහිටා ඇති අතර, පරමාදර්ශී මට්ටම 7,2 සහ 7,4 අතර වේ.
තටාකයේ ජලයේ pH අගය එතරම් වැදගත් වන්නේ ඇයි?
ආම්ලික, උදාසීන සහ ක්ෂාරීය pH අගයන්
pH අගයන්හි පරිමාණය වර්ගීකරණය
pH අගයන් මොනවාද?

pH පරිමාණය 1 සිට 14 දක්වා වන අතර pH 7 උදාසීන විසඳුමක් වේ.
එබැවින්, pH අගය 0 (අතිශයින් ආම්ලික) සහ 14 (අතිශයින් ක්ෂාරීය) අතර ලඝුගණක පරිමාණයකින් ප්රකාශිත අගයක් බව පෙනේ; ඒ අතර අපට 7 අගය උදාසීන ලෙස ලැයිස්තුගත කර ඇත.
pH පරිමාණයේ විශ්වීය pH දර්ශකය
ද්රව්යයක ආම්ලික හෝ ක්ෂාරීය pH මට්ටමක් ඇති බව එයින් අදහස් කරන්නේ කුමක්ද?
අම්ල සහ භෂ්ම යනු මොනවාද?
අම්ල සහ භෂ්ම යනු ස්වභාවධර්මයේ පවතින ද්රව්ය වන අතර ඒවායේ pH මට්ටම, එනම් ඒවායේ ආම්ලිකතාවය හෝ ක්ෂාරීයත්වය අනුව වෙන්කර හඳුනාගත හැකිය. ද්රව්ය ආම්ලික ද ක්ෂාරීය ද යන්න තීරණය කිරීම pH පරිමාණයෙන් මනිනු ලබන ආම්ලිකතාවයේ හෝ ක්ෂාරීයතාවයේ ප්රමාණයෙන් පාලනය වන අතර 0 (අතිශයින් ආම්ලික (අතිශයින් ක්ෂාරීය) සිට 14 දක්වා පරාසයක පවතී. කෙසේ වෙතත්, මේ දෙකම සාමාන්යයෙන් විඛාදනයට ලක්වන, බොහෝ විට විෂ සහිත ද්රව්ය වේ. කෙසේ වෙතත් කාර්මික හා මානව යෙදුම් ගණනාවක් ඇත.
ආම්ලික ද්රව්ය මොනවාද?
- අම්ල pH මට්ටම: pH අගය 7 ට වඩා අඩුය
pH අගය ආම්ලික බව එයින් අදහස් කරන්නේ කුමක්ද?
- යම් ද්රව්යයක් ආම්ලික බව යනු එහි H වලින් පොහොසත් බවයි+ (හයිඩ්රජන් අයන): pH අගය 7 ට වැඩි
- එබැවින්, අම්ල යනු pH අගය 7ට වඩා අඩු ද්රව්ය වේ. (ජලයේ pH අගය 7 ට සමාන, උදාසීන ලෙස සලකනු ලැබේ), එහි රසායන විද්යාව සාමාන්යයෙන් ජලය එකතු කිරීමේදී හයිඩ්රජන් අයන විශාල ප්රමාණයක් අඩංගු වේ. ඒවා සාමාන්යයෙන් ප්රෝටෝන අහිමි වීමෙන් වෙනත් ද්රව්ය සමඟ ප්රතික්රියා කරයි (H+).
උදාසීන ද්රව්ය මොනවාද?
- උදාසීන pH අගය: pH අගය 7-
pH අගය උදාසීන බව එයින් අදහස් කරන්නේ කුමක්ද?
- pH යනු ජලය කෙතරම් ආම්ලික/මූලිකද යන්න පිළිබඳ මිනුමක් වේ.
- පරාසය 0 සිට 14 දක්වා වන අතර, 7 මධ්යස්ථ වේ.
ක්ෂාරීය ද්රව්ය මොනවාද?
- පාදක හෝ ක්ෂාරීය pH අගය සහිත ද්රව්ය: pH අගය 7 ට වැඩි.
pH අගය ක්ෂාරීය වන විට එයින් අදහස් කරන්නේ කුමක්ද?
- ද්රව්යයක් ක්ෂාරීය යනු එය H හි දුර්වල බවයි+ (හෝ OH පදනම් වලින් පොහොසත්-, එච් උදාසීන කරයි+).
- මේ සියල්ල සඳහා, අනෙක් අතට, පදනම් යනු 7 ට වඩා වැඩි pH අගයක් සහිත ද්රව්ය වේ., ජලීය ද්රාවණවල සාමාන්යයෙන් හයිඩ්රොක්සයිල් අයන (OH-) අතරමැද දී. ඒවා ප්රබල ඔක්සිකාරක වීමට නැඹුරු වේ, එනම් අවට මාධ්යයෙන් ප්රෝටෝන සමඟ ප්රතික්රියා කරයි.
pH සහ pOH අගයන් අතර වෙනස්කම්
pH අගය සහ pOH අගය අතර වෙනස්කම්

සාමාන්ය pH අගය කුමක්ද?
- එක්තරා ආකාරයකින්, pH යනු මිනුමකි ද්රාවණයක ආම්ලිකතාවය හෝ ක්ෂාරීය මට්ටම තහවුරු කිරීමට භාවිතා කරයි. "p" යනු "විභවය" යන්නයි, ඒ නිසා pH ලෙස හැඳින්වේ: හයිඩ්රජන් විභවය.
pOH අගය යනු කුමක්ද?
- ඔබේ කොටස සඳහා. pOH යනු ද්රාවණයක ඇති හයිඩ්රොක්සයිල් අයන සාන්ද්රණයේ මිනුමක් වේ. එය හයිඩ්රොක්සිල් අයන සාන්ද්රණයේ පාදක 10 සෘණ ලඝුගණකය ලෙස ප්රකාශ වන අතර pH අගය මෙන් නොව ද්රාවණයක ක්ෂාරීය මට්ටම මැනීමට භාවිතා කරයි.
නිෂ්පාදන පිරිසිදු කිරීමේදී pH පරිමාණයේ වැදගත්කම කුමක්ද?
pH අගය සහ මීටර වර්ග මනින ආකාරය
තටාකයේ pH අගය මැන ගන්නේ කෙසේද?

රතු ගෝවා සමඟ ගෙදර හැදූ pH දර්ශකයක් සාදන්න

තටාකයේ pH අගය මැන ගන්නේ කෙසේද, කොපමණ වාර ගණනක් සහ මීටර් වර්ග
pH අගය ගණනය කරන්නේ කෙසේද?

pH පරිමාණය ගණනය කරනු ලබන්නේ සෘණ ලඝුගණකයක් මගිනි.
pH අගය ලඝුගණක වේ
pH තමයි ලඝුගණකය H අයන සාන්ද්රණයෙන්+, ලකුණ වෙනස් කිරීමත් සමඟ: ඒ හා සමානව, pOH ලෙස අර්ථ දැක්වේ ලඝුගණකය OH අයන සාන්ද්රණයෙන්-, ලකුණ වෙනස් කිරීමත් සමඟ: පහත සම්බන්ධතාව අතර ස්ථාපිත කළ හැක pH සහ pOH. ජලයේ අයනික නිෂ්පාදනයේ ප්රකාශනයෙන් ආරම්භ වේ (Kw):
ලඝුගණක pH සූත්රය
- ලොග් pH සූත්රය: pH සමීකරණය භාවිතයෙන් pH අගය ගණනය කරන්න: pH = -log[H3O+].
pH අගය ලඝුගණක බව එයින් අදහස් කරන්නේ කුමක්ද?
pH අගය ලඝුගණක වීම යන්නෙන් අදහස් වන්නේ පරිමාණයේ සෑම ඒකකයක් අතරම 10 ක වෙනසක් ඇති බවයි.
- ඉතින්, මෙයින් අදහස් කරන්නේ pH 5 pH 10 ට වඩා 6 ගුණයක් ආම්ලික වන අතර pH 4 pH 100 ට වඩා 6 ගුණයක් ආම්ලික වේ.
ලඝුගණක සමඟ pH අගය ගණනය කරන්නේ කෙසේද?
පරිමාණය pH අගය ගණනය කෙරේ a හරහා ලඝුගණකය සෘණ. ඒ ලඝුගණකය සෘණ සරලව පෙන්නුම් කරන්නේ සංඛ්යාවක් කොපමණ වාර ගණනක් බෙදිය යුතුද යන්නයි. යන සමීකරණය pH පහත පරිදි ලිවිය හැකිය: pH = -log[H3O+]. සමහර විට සමීකරණය මෙසේ ලියා ඇත: pH = -ලොග්[එච්+].
pH අගය පරිමාණය වර්ධනය වීමට හේතුව: ජලය සම්මතයක් ලෙස ගනිමින් pH පරිමාණය සංවර්ධනය කරන ලදී.

- ජල මවුල 1 ක මවුල 5,50,000,000 ක් පමණක් H+ එකක් සහ OH- එකක් බවට අයනීකරණය වන බව පර්යේෂණාත්මක සත්යයකි.
- මෙය ජලය ලීටර් 10.000.000 ක හයිඩ්රජන් අයන ග්රෑම් එකක අනුපාතයට සමාන වේ.
- එබැවින් ජලය ලීටරයක H+ ග්රෑම් එකකින් 1/10.000.000 (හෝ) 1/107 ක් අඩංගු වේ. එදිනෙදා භාවිතය සඳහා, pH සංකේතය ඉදිරියෙන් තබා, 'විභව' රූපය පමණක් භාවිතා කරන ලදී.
තටාක pH කැල්කියුලේටරය
තටාකයේ ජලයේ pH අගය පහළට හෝ ඉහළට යන්නේ ඇයි?
තටාකයේ pH අගය වැඩි කරන්නේ කෙසේද සහ මට්ටම අඩු නම් කුමක් සිදුවේද?
pH සංචිතයේ ප්රතිවිපාක සහ ඉහළ pH හේතු
pH අගය නිර්දේශිත අගයට වඩා වැඩි නම් කුමක් සිදුවේද?
ඉහළ pH සංචිතයේ ප්රතිවිපාක: තටාකයේ pH අගය වැඩි නම් කුමක් සිදුවේද?

- පළමුවෙන්ම, ඉහළ pH සංචිතයේ ප්රතිවිපාක ජලය නිසියාකාරව සංසරණය වීමට අපහසු වන අතර බොහෝ විට, එය සමහර වර්ගවල පෙරහන් හෝ ජල තාපක භාවිතා කිරීමෙන් පැන නගින ගැටළුවකි.
- අපගේ ශරීරයේ රෝග ලක්ෂණ වියළි හා කෝපයට පත් සම වේ.
- ඒ හා සමානව, වළාකුළු පිරි ජලය සමහර විට ජලය විෂබීජහරණය කිරීමට ක්ලෝරීන් ප්රමාණවත් නොවන ප්රමාණයක් හෝ දෛනික භාවිතයේ නිෂ්පාදනයක් භාවිතා කිරීමෙන් තටාකයේ pH අගය වෙනස් කරයි.
- එය ප්රමාණවත් නොවූවාක් මෙන්, ඉහළ pH අගය ස්ඵටික පැහැදිලි ජලයෙන් අවසන් වන තටාකයේ දෙහි තැන්පතු සෑදීමට දිරිගන්වනු ඇත. මෙම හුණු තැන්පතු පයිප්පවල සහ අනෙකුත් ස්ථාපනයන්හි තැන්පත් වී ඇති අතර, ඒවායේ ස්ථාවරත්වය සහ නිසි ක්රියාකාරීත්වයට බලපානු ඇත. ඔවුන් තටාකයේ පෙනුම සහ පිරිසිදුකම වෙනස් කරමින් බිත්ති සහ බිම්වලට ද ඇලී සිටිනු ඇත.
පහතින්, එය ඔබට උනන්දුවක් දක්වන්නේ නම්, අපි ඔබට සබැඳියක් සපයන්නෙමු පිහිනුම් තටාකවල pH අගය ඉහළ යාමේ සියලු ප්රතිවිපාක සහ ඒවාට ඇති විය හැකි හේතු විශ්ලේෂණය කරන පිටුව.











