
Lapas satura rādītājs
En Labi, baseina reforma, šajā sadaļā pH līmeņa peldbaseini mēs ārstēsim atšķirība starp ph un poh baseina ūdens vērtībās.
Kāds ir pH līmenis baseinā un kādam jābūt tā līmenim?

Ko nozīmē ideāls pH peldbaseiniem (7,2-7,4)
Akronīms pH apzīmē potenciālo ūdeņradi un ir mērs, kas norāda ūdens skābumu vai bāziskumu.
Tad, pH attiecas uz ūdeņraža potenciālu, vērtību, kas atbilst ūdeņraža jonu koncentrācijai jūsu baseina ūdenī un tāpēc ir koeficients, kas norāda ūdens skābuma vai bāziskuma pakāpi. Tāpēc pH ir atbildīgs par H+ jonu koncentrācijas norādīšanu ūdenī, nosakot tā skābo vai bāzisko raksturu.
Peldbaseina ūdens pH vērtību skala


Kādas vērtības ir iekļautas baseina ūdens pH mērīšanas skalā?
- PH mērīšanas skala ietver vērtības no 0 līdz 14.
- Jo īpaši 0 ir skābākā, 14 visbāziskākā un neitrāls pH ir 7.
- Šo mērījumu nosaka brīvo ūdeņraža jonu (H+) skaits vielā.

Kāpēc mums ir nepieciešams pH?
pH ir mērs, ko izmanto, lai norādītu ūdens šķīduma skābumu vai bāziskumu. Tas, vai ūdens šķīdums reaģē kā skābe vai bāze, ir atkarīgs no ūdeņraža jonu (H+) satura.
Tomēr pat ķīmiski tīrs un neitrāls ūdens satur dažus ūdeņraža jonus ūdens pašdisociācijas dēļ.
Ir zināms, ka līdzsvarā standarta apstākļos (750 mmHg un 25°C) 1 l tīra ūdens satur mol
y
mol
jonus, tāpēc ūdens standarta temperatūrā un spiedienā (STP) pH ir 7.
Ko darīt, ja mūsu baseina pH NAV regulēts

Ziniet augsta pH baseina sekas un augsta pH cēloņus jūsu baseinā

Kā paaugstināt baseina pH un kas notiek, ja tas ir zems

Kā pazemināt augstu vai sārmainu baseina pH
Rokasgrāmatas par to, kā veikt baseina apkopi papildus pH: ūdens tīrīšana un dezinfekcija

Noderīgs ceļvedis, lai uzzinātu, kā tīrīt baseinu

Rokasgrāmata, kā uzturēt baseinu ar ūdeni ideālā stāvoklī
Skāba, neitrāla un sārma pH vērtības
PH vērtību skalas klasifikācija
Kādas ir pH vērtības

pH skala ir no 1 līdz 14, un pH 7 ir neitrāls šķīdums.
Tātad, izrādās, ka pH ir vērtība, kas tiek izteikta logaritmiskā skalā starp vērtībām 0 (ļoti skābs) un 14 (ļoti sārmains); Pa vidu mēs atrodam vērtību 7, kas kataloģizēta kā neitrāla.
pH skalas universāls pH indikators
Ko nozīmē, ka vielai ir skābs vai sārmains pH līmenis?
Kas ir skābes un bāzes?
Skābes un bāzes ir vielas, kas eksistē dabā un atšķiras pēc pH līmeņa, tas ir, pēc skābuma vai sārmainības pakāpes. To, vai vielas ir skābas vai sārmainas, nosaka skābuma vai sārmainības pakāpe, ko mēra ar pH skalu un ir robežās no 0 (ļoti skābs līdz 14 (ļoti sārmains). Tomēr abas parasti ir kodīgas, bieži toksiskas vielas, kas tomēr tiem ir daudz rūpniecisku un cilvēku pielietojumu.
Kas ir skābās vielas?
- Skābes pH līmenis: pH mazāks par 7
Ko tas nozīmē, ka pH vērtība ir skāba?
- Tas, ka viela ir skāba, nozīmē, ka tā ir bagāta ar H+ (ūdeņraža joni): pH lielāks par 7
- Tāpēc Skābes ir vielas, kuru pH ir mazāks par 7. (ūdens pH ir vienāds ar 7, tiek uzskatīts par neitrālu), kura ķīmiskā viela parasti satur lielu daudzumu ūdeņraža jonu, pievienojot ūdeni. Tās parasti reaģē ar citām vielām, zaudējot protonus (H+).
Kas ir neitrālas vielas?
- Neitrālā pH vērtība: pH vienāds ar 7-
Ko tas nozīmē, ka pH vērtība ir neitrāla?
- pH ir ūdens skābuma/bāziskā satura rādītājs.
- Diapazons ir no 0 līdz 14, un 7 ir neitrāli.
Kas ir sārmainas vielas?
- Vielas ar bāzes vai sārmainu pH: pH lielāks par 7.
Ko tas nozīmē, ja pH vērtība ir sārmaina?
- Tas, ka viela ir sārmaina, nozīmē, ka tajā ir maz H+ (vai bagāts ar OH bāzēm-, kas neitralizē H+).
- Par šo visu No otras puses, bāzes ir vielas, kuru pH ir lielāks par 7., kas ūdens šķīdumos parasti nodrošina hidroksiljonus (OH-) vidū. Tie mēdz būt spēcīgi oksidētāji, tas ir, tie reaģē ar protoniem no apkārtējās vides.
Atšķirības starp pH un pOH vērtībām

Kā tie ir saistīti un kādas ir atšķirības starp ph un poh mērījumiem?
Protams, jonu aktivitāte ir atkarīga no jonu koncentrācijas un tas ir aprakstīts vienādojumā
pH/poH jonu aktivitātes vienādojums
kur, – ūdeņraža jonu aktivitāte
– ūdeņraža jona aktivitātes koeficients
– ūdeņraža jonu koncentrācija
Aktivitātes koeficients ir jonu koncentrācijas funkcija un tuvojas 1, šķīdumam kļūstot arvien atšķaidītākam.
Atšķaidītiem (ideāliem) šķīdumiem izšķīdušās vielas standartstāvoklis ir 1,00 M, tāpēc tās molaritāte ir vienāda ar tās aktivitāti.
Tādējādi lielākajai daļai problēmu, kas paredz ideālus risinājumus, mēs varam izmantot logaritmu uz molārās koncentrācijas 10. bāzi, nevis aktivitāti.
Atšķirības starp pH un pOH vērtību

Kāda ir normāla pH vērtība?
- Savā ziņā pH ir pasākums, kas izmanto, lai noteiktu šķīduma skābuma vai sārmainības līmeni. “p” apzīmē “potenciāls”, tāpēc pH tiek saukts par ūdeņraža potenciālu.
Kāda ir pOH vērtība?
- No savas puses. pOH ir hidroksiljonu koncentrācijas mērs šķīdumā. To izsaka kā hidroksiljonu koncentrācijas 10 bāzes negatīvo logaritmu un atšķirībā no pH izmanto šķīduma sārmainības līmeņa mērīšanai.

Kā aprēķina pH vai pOH vērtību?
Kāda ir ph skalas vērtību formula?
- Kā jau zināms, zinātnes jomā, pH ir pasākums de joni iekšā de risinājums. Jums var nākties aprēķināt pH pamatojoties uz koncentrāciju. Aprēķiniet pH Izmantojot vienādojumu pH: pH = -log[H3O+].
Kāda ir formula pOH aprēķināšanai?
- Tāpat arī pOH (vai OH potenciāls) ir šķīduma bāziskuma vai sārmainības mērs. Arī se izmanto pH = – log [H3O+], lai izmērītu hidronija jonu koncentrāciju [H3O+].

Galvenie vienādojumi pH vai pOH vērtības aprēķināšanai
- pH=-log[H3O+]
- pOH=-log[OH-]
- [H3O+] = 10-pH
- [ak-] = 10-pOH
- pH + pOH =pKw = 14.00 pie 25 °C.
Kāda ir atšķirība starp pH vērtību skalu un pOH skalu?
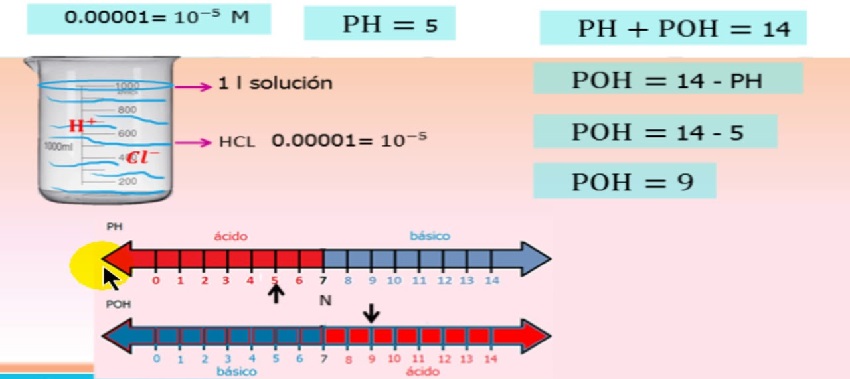
Nevienādības starp pH skalas vērtībām
- No vienas puses, pH skala dod skābes vērtības no 1 līdz 6, savukārt pOH skala dod skābes vērtības no 8 līdz 14.
- Un otrādi, pH skala dod pamatvērtības no 8 līdz 14, bet pOH skala dod pamatvērtības no 1 līdz 6.
ph un pOH logaritma mēroga attiecības ar to vērtībām
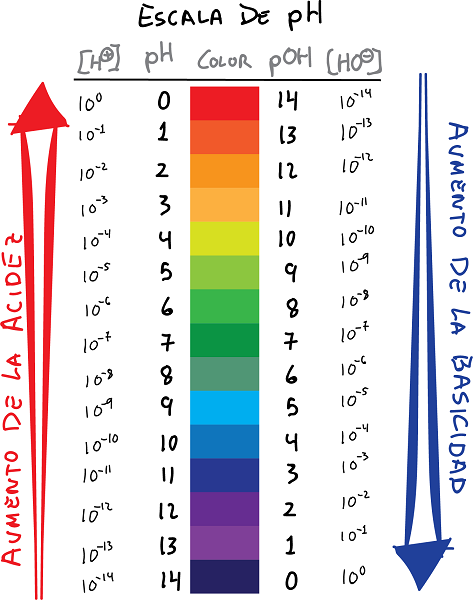
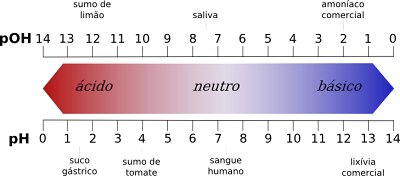
ph un pOH mēroga savienojums ar krāsām un vērtībām
- pH ir H jonu koncentrācijas logaritms+, ar mainītu zīmi:
- Līdzīgi definējiet pOH kā OH jonu koncentrācijas logaritms-, ar mainītu zīmi: Starp var izveidot šādas attiecības pH un pOH.
- Pamatā pH vērtības dod ūdeņraža jonu koncentrācijas negatīvo logaritmu, bet pOH vērtība – hidroksīda jonu koncentrācijas negatīvo logaritmu.
Atšķirība starp pH un pOH vērtību skalu
Neatbilstības starp ph vērtību tabulu un pOH vērtību
Pēc tam mēs jums piedāvājam filmu, kurā varat redzēt, ka pH mēra ūdeņraža jonu koncentrāciju, bet pOH mēra hidroksilanjonu vai hidroksīda jonu koncentrāciju.


