
ດັດຊະນີຂອງເນື້ອໃນຂອງຫນ້າ
En ການປະຕິຮູບສະນຸກເກີ Ok, ໃນພາກນີ້ພາຍໃນ ສະລອຍນ້ຳລະດັບ pH ພວກເຮົາຈະປິ່ນປົວ ຄວາມແຕກຕ່າງລະຫວ່າງ ph ແລະ poh ໃນຄ່ານ້ໍາສະນຸກເກີ.
pH ໃນສະນຸກເກີແມ່ນຫຍັງແລະລະດັບຂອງມັນຄວນຈະເປັນແນວໃດ?

pH ທີ່ເຫມາະສົມຫມາຍຄວາມວ່າແນວໃດສໍາລັບສະລອຍນ້ໍາ (7,2-7,4)
pH ຫຍໍ້ມາຈາກ hydrogen ທີ່ມີທ່າແຮງແລະເປັນມາດຕະການທີ່ຊີ້ບອກເຖິງຄວາມເປັນກົດຫຼືພື້ນຖານຂອງນ້ໍາ.
ດັ່ງນັ້ນ, pH ຫມາຍເຖິງທ່າແຮງຂອງ hydrogen, ເປັນມູນຄ່າທີ່ສອດຄ່ອງກັບຄວາມເຂັ້ມຂົ້ນຂອງ hydrogen ions ໃນນ້ໍາໃນສະນຸກເກີຂອງທ່ານແລະດັ່ງນັ້ນແມ່ນຄ່າສໍາປະສິດທີ່ຊີ້ບອກລະດັບຂອງກົດຫຼືພື້ນຖານຂອງນ້ໍາ. ດັ່ງນັ້ນ, pH ແມ່ນຮັບຜິດຊອບໃນການຊີ້ໃຫ້ເຫັນຄວາມເຂັ້ມຂົ້ນຂອງ H + ions ໃນນ້ໍາ, ກໍານົດລັກສະນະເປັນກົດຫຼືພື້ນຖານຂອງມັນ.
ຂະຫນາດຂອງຄ່າ pH ຂອງນ້ໍາສະລອຍນ້ໍາ


ຂະຫນາດການວັດແທກ pH ຂອງນ້ໍາສະນຸກເກີປະກອບມີຄ່າໃດ?
- ຂະຫນາດການວັດແທກ pH ປະກອບມີຄ່າຈາກ 0 ຫາ 14.
- ໂດຍສະເພາະແມ່ນ 0 ເປັນອາຊິດທີ່ສຸດ, 14 ເປັນພື້ນຖານທີ່ສຸດແລະການວາງ pH ກາງທີ່ 7.
- ການວັດແທກນີ້ແມ່ນຖືກກໍານົດໂດຍຈໍານວນຂອງ hydrogen ions ຟຣີ (H+) ໃນສານ.

ເປັນຫຍັງພວກເຮົາຕ້ອງການ pH?
pH ແມ່ນມາດຕະການທີ່ໃຊ້ເພື່ອກໍານົດຄວາມເປັນກົດຫຼືພື້ນຖານຂອງການແກ້ໄຂນ້ໍາ. ບໍ່ວ່າຈະເປັນການແກ້ໄຂທີ່ມີນ້ໍາປະຕິກິລິຍາເປັນອາຊິດຫຼືພື້ນຖານແມ່ນຂຶ້ນກັບເນື້ອໃນຂອງ hydrogen ions (H+).
ຢ່າງໃດກໍຕາມ, ເຖິງແມ່ນວ່ານ້ໍາບໍລິສຸດແລະເປັນກາງທາງເຄມີກໍ່ມີບາງ ions hydrogen ເນື່ອງຈາກການແຍກຕົວຂອງນ້ໍາ.
ມັນເປັນທີ່ຮູ້ຈັກວ່າຢູ່ໃນຄວາມສົມດຸນພາຍໃຕ້ເງື່ອນໄຂມາດຕະຖານ (750 mmHg ແລະ 25 ° C), 1 L ຂອງນ້ໍາບໍລິສຸດປະກອບດ້ວຍ. ຕ່ອມ
y
ຕ່ອມ
ດັ່ງນັ້ນ, ion ນ້ໍາໃນອຸນຫະພູມແລະຄວາມກົດດັນມາດຕະຖານ (STP) ມີ pH ຂອງ 7.
ຈະເຮັດແນວໃດເມື່ອ pH ຂອງສະນຸກເກີຂອງພວກເຮົາບໍ່ໄດ້ຖືກຄວບຄຸມ

ຮູ້ຜົນສະທ້ອນ pH ສູງແລະສາເຫດຂອງ pH ສູງໃນສະນຸກເກີຂອງທ່ານ

ວິທີການຍົກສູງ pH ຂອງສະນຸກເກີແລະສິ່ງທີ່ເກີດຂຶ້ນຖ້າຫາກວ່າມັນຕ່ໍາ

ວິທີການຫຼຸດລົງ pH ສູງຫຼືເປັນດ່າງຂອງສະລອຍນ້ໍາ
ຄໍາແນະນໍາກ່ຽວກັບວິທີການບໍາລຸງຮັກສາສະລອຍນ້ໍານອກເຫນືອຈາກ pH: ການທໍາຄວາມສະອາດນ້ໍາແລະການຂ້າເຊື້ອ

ຄູ່ມືທີ່ເປັນປະໂຫຍດເພື່ອຮູ້ວິທີການເຮັດຄວາມສະອາດສະລອຍນ້ໍາ

ຄູ່ມືການຮັກສາສະລອຍນ້ໍາທີ່ມີນ້ໍາຢູ່ໃນສະພາບທີ່ສົມບູນແບບ
ຄ່າ pH ຂອງອາຊິດ, ເປັນກາງ ແລະເປັນດ່າງ
ການຈັດປະເພດຂະຫນາດຂອງຄ່າ pH
ຄ່າ pH ແມ່ນຫຍັງ

ຂະຫນາດ pH ແມ່ນຕັ້ງແຕ່ 1 ຫາ 14, ດ້ວຍ pH 7 ເປັນການແກ້ໄຂທີ່ເປັນກາງ.
ດັ່ງນັ້ນ, ມັນ turns ໃຫ້ເຫັນວ່າ pH ເປັນຄ່າທີ່ສະແດງອອກດ້ວຍຂະຫນາດ logarithmic ລະຫວ່າງຄ່າ 0 (ອາຊິດທີ່ສຸດ) ແລະ 14 (ເປັນດ່າງຫຼາຍ); ໃນລະຫວ່າງພວກເຮົາຊອກຫາຄ່າ 7 ທີ່ຖືກຈັດໃສ່ເປັນກາງ.
ຕົວຊີ້ວັດ pH ລະດັບ pH ທົ່ວໄປ
ມັນ ໝາຍ ຄວາມວ່າສານໃດ ໜຶ່ງ ມີລະດັບ pH ທີ່ເປັນກົດຫຼືເປັນດ່າງ?
ອາຊິດແລະຖານແມ່ນຫຍັງ?
ອາຊິດແລະຖານແມ່ນສານທີ່ມີຢູ່ໃນທໍາມະຊາດແລະຖືກຈໍາແນກໂດຍລະດັບ pH ຂອງພວກມັນ, ນັ້ນແມ່ນ, ໂດຍລະດັບຄວາມສົ້ມຫຼືຄວາມເປັນດ່າງຂອງພວກມັນ. ການກໍານົດວ່າສານທີ່ເປັນກົດຫຼືເປັນດ່າງແມ່ນຄຸ້ມຄອງໂດຍລະດັບຄວາມສົ້ມຫຼືຄວາມເປັນດ່າງທີ່ວັດແທກໂດຍຜ່ານຂະຫນາດ pH ແລະມີລະດັບຈາກ 0 (ອາຊິດຫຼາຍເຖິງ 14 (ເປັນດ່າງຫຼາຍ)). ຢ່າງໃດກໍຕາມ, ມີການນໍາໃຊ້ອຸດສາຫະກໍາແລະມະນຸດຈໍານວນຫລາຍ.
ສານອາຊິດແມ່ນຫຍັງ?
- ລະດັບ pH ຂອງອາຊິດ: pH ຫນ້ອຍກວ່າ 7
ມັນຫມາຍຄວາມວ່າຄ່າ pH ເປັນອາຊິດແນວໃດ?
- ສານທີ່ເປັນກົດ ໝາຍ ຄວາມວ່າອຸດົມໄປດ້ວຍ H+ (ໄອອອນໄຮໂດຣເຈນ): pH ສູງກວ່າ 7
- ດັ່ງນັ້ນ, ອາຊິດແມ່ນສານທີ່ມີ pH ຕ່ໍາກວ່າ 7. (pH ຂອງນ້ໍາເທົ່າກັບ 7, ພິຈາລະນາເປັນກາງ), ເຄມີສາດໂດຍທົ່ວໄປປະກອບດ້ວຍຈໍານວນຂະຫນາດໃຫຍ່ຂອງ hydrogen ions ໃນເວລາທີ່ເພີ່ມນ້ໍາ. ປົກກະຕິແລ້ວພວກມັນປະຕິກິລິຍາກັບສານອື່ນໆໂດຍການສູນເສຍໂປຣຕິນ (H+).
ສານທີ່ເປັນກາງແມ່ນຫຍັງ?
- ຄ່າ pH ເປັນກາງ: pH ເທົ່າກັບ 7-
ມັນຫມາຍຄວາມວ່າຄ່າ pH ເປັນກາງແນວໃດ?
- pH ແມ່ນການວັດແທກວິທີການເປັນກົດ / ພື້ນຖານຂອງນ້ໍາ.
- ຂອບເຂດແມ່ນຕັ້ງແຕ່ 0 ຫາ 14, ໂດຍ 7 ເປັນກາງ.
ສານທີ່ເປັນດ່າງແມ່ນຫຍັງ?
- ສານທີ່ມີ pH ພື້ນຖານຫຼືເປັນດ່າງ: pH ສູງກວ່າ 7.
ມັນຫມາຍຄວາມວ່າແນວໃດເມື່ອຄ່າ pH ເປັນດ່າງ?
- ວ່າສານທີ່ເປັນດ່າງຫມາຍຄວາມວ່າມັນບໍ່ດີໃນ H+ (ຫຼືອຸດົມສົມບູນໃນ OH bases-, ເຊິ່ງ neutralize H+).
- ສຳ ລັບສິ່ງທັງ ໝົດ ນີ້, ໃນທາງກົງກັນຂ້າມ, ພື້ນຖານແມ່ນສານທີ່ມີ pH ສູງກວ່າ 7., ເຊິ່ງໃນການແກ້ໄຂທີ່ມີນ້ໍາມັກຈະສະຫນອງ ions hydroxyl (OH-) ຢູ່ໃນກາງ. ພວກເຂົາເຈົ້າມີແນວໂນ້ມທີ່ຈະເປັນສານຕ້ານອະນຸມູນອິສະລະທີ່ມີອໍານາດ, ນັ້ນແມ່ນ, ພວກມັນປະຕິກິລິຍາກັບ protons ຈາກສື່ອ້ອມຂ້າງ.
ຄວາມແຕກຕ່າງລະຫວ່າງຄ່າ pH ແລະ pOH

ມີຄວາມກ່ຽວຂ້ອງກັນແນວໃດ ແລະຄວາມແຕກຕ່າງລະຫວ່າງການວັດແທກ ph ແລະ poh ແມ່ນຫຍັງ?
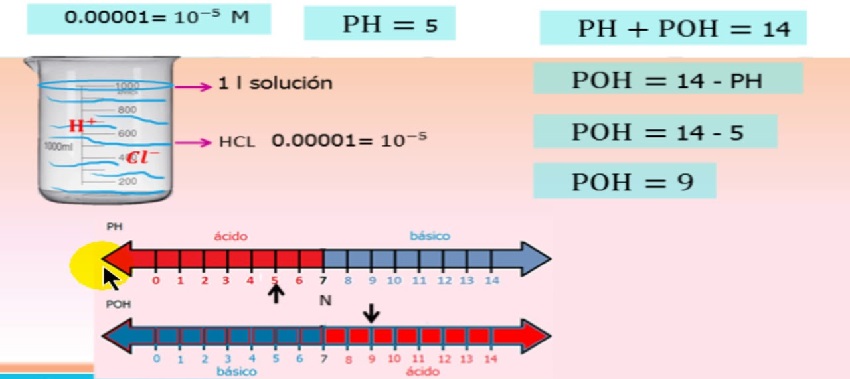
ແນ່ນອນ, ກິດຈະກໍາຂອງ ions ແມ່ນຂຶ້ນກັບຄວາມເຂັ້ມຂົ້ນຂອງ ion ແລະນີ້ໄດ້ຖືກອະທິບາຍໄວ້ໃນສົມຜົນ
ສົມຜົນຂອງກິດຈະກໍາ pH/poH ion
ບ່ອນໃດ, - ກິດຈະກໍາ hydrogen ion
- ຄ່າສໍາປະສິດກິດຈະກໍາຂອງ hydrogen ion
- ຄວາມເຂັ້ມຂຸ້ນຂອງ hydrogen ion
ຄ່າສໍາປະສິດກິດຈະກໍາແມ່ນຫນ້າທີ່ຂອງຄວາມເຂັ້ມຂົ້ນຂອງ ion ແລະເຂົ້າຫາ 1 ຍ້ອນວ່າການແກ້ໄຂຈະກາຍເປັນເຈືອຈາງຫຼາຍຂຶ້ນ.
ສໍາລັບການແກ້ໄຂທີ່ເຈືອຈາງ (ທີ່ເຫມາະສົມ), ສະຖານະມາດຕະຖານຂອງສານລະລາຍແມ່ນ 1,00 M, ດັ່ງນັ້ນ molarity ຂອງມັນເທົ່າກັບກິດຈະກໍາຂອງມັນ.
ດັ່ງນັ້ນ, ສໍາລັບບັນຫາສ່ວນໃຫຍ່ທີ່ສົມມຸດວ່າການແກ້ໄຂທີ່ເຫມາະສົມພວກເຮົາສາມາດໃຊ້ logarithm ກັບຖານ 10 ຂອງຄວາມເຂັ້ມຂົ້ນຂອງ molar, ບໍ່ແມ່ນກິດຈະກໍາ.
ຄວາມແຕກຕ່າງລະຫວ່າງຄ່າຂອງ pH ແລະ pOH

ຄ່າ pH ປົກກະຕິແມ່ນຫຍັງ?
- ໂດຍວິທີທາງການ, pH ແມ່ນການວັດແທກ ໃຊ້ເພື່ອສ້າງລະດັບຄວາມສົ້ມ ຫຼືຄວາມເປັນດ່າງຂອງການແກ້ໄຂ. "p" ຫຍໍ້ມາຈາກ "ທ່າແຮງ", ນັ້ນແມ່ນເຫດຜົນທີ່ວ່າ pH ຖືກເອີ້ນວ່າ: ທ່າແຮງຂອງ hydrogen.
ຄ່າ pOH ແມ່ນຫຍັງ?
- ສໍາລັບພາກສ່ວນຂອງທ່ານ. pOH ແມ່ນການວັດແທກຄວາມເຂັ້ມຂຸ້ນຂອງ hydroxyl ions ໃນການແກ້ໄຂ. ມັນສະແດງອອກເປັນພື້ນຖານ 10 logarithm ລົບຂອງຄວາມເຂັ້ມຂຸ້ນຂອງ hydroxyl ion ແລະ, ບໍ່ເຫມືອນກັບ pH, ຖືກນໍາໃຊ້ເພື່ອວັດແທກລະດັບຄວາມເປັນດ່າງຂອງການແກ້ໄຂ.

ຄ່າ pH ຫຼື pOH ຖືກຄິດໄລ່ແນວໃດ?
ສູດສໍາລັບຄ່າ ph scale ແມ່ນຫຍັງ?
- ດັ່ງທີ່ມັນເປັນທີ່ຮູ້ຈັກແລ້ວ, ໃນຂົງເຂດວິທະຍາສາດ, ໄດ້ pH ແມ່ນມາດຕະການ de ion ພາຍໃນ de ການແກ້ໄຂ. ທ່ານອາດຈະຕ້ອງ ຄິດໄລ່ pH ອີງໃສ່ຄວາມເຂັ້ມຂົ້ນ. ຄິດໄລ່ pH ການນໍາໃຊ້ສົມຜົນຂອງ pH: pH = -log[H3O+].
ສູດຄິດໄລ່ pOH ແມ່ນຫຍັງ?
- ນອກຈາກນີ້ pOH (ຫຼືທ່າແຮງ OH) ແມ່ນມາດຕະການຂອງພື້ນຖານຫຼືຄວາມເປັນດ່າງຂອງການແກ້ໄຂ. ນອກຈາກນີ້ se ໃຊ້ pH = – log [H3O+] ເພື່ອວັດແທກຄວາມເຂັ້ມຂຸ້ນຂອງ hydronium ion [H3O+].

ສົມຜົນຫຼັກເພື່ອຄິດໄລ່ຄ່າ pH ຫຼື pOH
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [ໂອ-] = 10-pOH
- pH + pOH =pKw = 14.00 ອຸນຫະພູມ 25°C.
ຄວາມແຕກຕ່າງລະຫວ່າງຂະຫນາດຂອງຄ່າ pH ແລະ pOH ແມ່ນຫຍັງ?
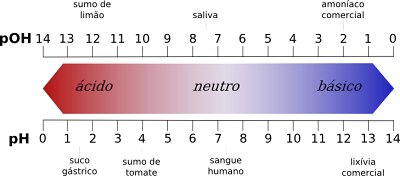
ຄວາມບໍ່ສະເຫມີພາບລະຫວ່າງຄ່າຂອງຂະຫນາດ pH
- ໃນດ້ານຫນຶ່ງ, ຂະຫນາດ pH ໃຫ້ຄ່າອາຊິດຈາກ 1 ຫາ 6 ໃນຂະນະທີ່ຂະຫນາດ pOH ໃຫ້ຄ່າອາຊິດຈາກ 8 ຫາ 14.
- ກົງກັນຂ້າມ, ຂະຫນາດ pH ໃຫ້ຄ່າພື້ນຖານຈາກ 8 ຫາ 14, ໃນຂະນະທີ່ຂະຫນາດ pOH ໃຫ້ຄ່າພື້ນຖານຈາກ 1 ຫາ 6.
ຄວາມສຳພັນຂະໜາດ logarithm ຂອງ ph ແລະ pOH ກັບຄ່າຂອງພວກມັນ
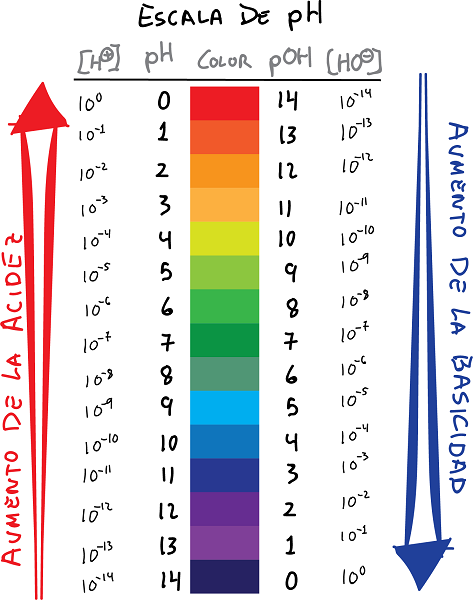
ການເຊື່ອມຕໍ່ຂະຫນາດ ph ແລະ pOH ກັບສີແລະຄ່າ
- pH ເປັນ logarithm ຂອງຄວາມເຂັ້ມຂຸ້ນຂອງ H ions+, ມີການປ່ຽນແປງສັນຍານ:
- ເຊັ່ນດຽວກັນ, ກໍານົດ pOH ເປັນ logarithm ຂອງຄວາມເຂັ້ມຂຸ້ນຂອງ OH ion-, ມີການປ່ຽນແປງສັນຍານ: ການພົວພັນດັ່ງຕໍ່ໄປນີ້ສາມາດໄດ້ຮັບການສ້າງຕັ້ງຂຶ້ນລະຫວ່າງ pH ແລະໄດ້ pOH.
- ໂດຍພື້ນຖານແລ້ວ, ຄ່າ pH ໃຫ້ຄ່າທາງລົບຂອງ logarithm ຂອງຄວາມເຂັ້ມຂົ້ນຂອງ hydrogen ion, ໃນຂະນະທີ່ຄ່າ pOH ໃຫ້ຄ່າ logarithm ລົບຂອງຄວາມເຂັ້ມຂົ້ນຂອງ hydroxide ion.
ຄວາມແຕກຕ່າງລະຫວ່າງຂະຫນາດຂອງ pH ແລະ pOH
ຄວາມແຕກຕ່າງລະຫວ່າງຕາຕະລາງຄ່າ ph ແລະຄ່າ pOH
ຫຼັງຈາກນັ້ນ, ພວກເຮົາໃຫ້ທ່ານມີຮູບເງົາທີ່ທ່ານສາມາດເຫັນໄດ້ວ່າ pH ວັດແທກຄວາມເຂັ້ມຂົ້ນຂອງ ions hydrogen, ໃນຂະນະທີ່ pOH ວັດແທກຄວາມເຂັ້ມຂຸ້ນຂອງ hydroxyl anions ຫຼື hydroxide ions.


