
ಪುಟದ ವಿಷಯಗಳ ಸೂಚ್ಯಂಕ
En ಸರಿ ಪೂಲ್ ಸುಧಾರಣೆ, ಒಳಗೆ ಈ ವಿಭಾಗದಲ್ಲಿ pH ಮಟ್ಟದ ಈಜುಕೊಳಗಳು ನಾವು ಚಿಕಿತ್ಸೆ ನೀಡುತ್ತೇವೆ ಪೂಲ್ ನೀರಿನ ಮೌಲ್ಯಗಳಲ್ಲಿ ph ಮತ್ತು poh ನಡುವಿನ ವ್ಯತ್ಯಾಸ.
ಪೂಲ್ನಲ್ಲಿ pH ಎಂದರೇನು ಮತ್ತು ಅದರ ಮಟ್ಟಗಳು ಹೇಗಿರಬೇಕು?

ಈಜುಕೊಳಗಳಿಗೆ ಆದರ್ಶ pH ಅರ್ಥವೇನು (7,2-7,4)
ಸಂಕ್ಷಿಪ್ತ ರೂಪ pH ಸಂಭಾವ್ಯ ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತದೆ ಮತ್ತು ಇದು ನೀರಿನ ಆಮ್ಲತೆ ಅಥವಾ ಮೂಲಭೂತತೆಯನ್ನು ಸೂಚಿಸುವ ಅಳತೆಯಾಗಿದೆ.
ಆದ್ದರಿಂದ, pH ಹೈಡ್ರೋಜನ್ನ ಸಂಭಾವ್ಯತೆಯನ್ನು ಸೂಚಿಸುತ್ತದೆ, ಇದು ನಿಮ್ಮ ಕೊಳದಲ್ಲಿನ ನೀರಿನಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಗೆ ಅನುರೂಪವಾಗಿರುವ ಮೌಲ್ಯವಾಗಿದೆ ಮತ್ತು ಆದ್ದರಿಂದ ಇದು ನೀರಿನ ಆಮ್ಲೀಯತೆ ಅಥವಾ ಮೂಲಭೂತತೆಯ ಮಟ್ಟವನ್ನು ಸೂಚಿಸುವ ಗುಣಾಂಕವಾಗಿದೆ. ಆದ್ದರಿಂದ, pH ನೀರಿನಲ್ಲಿ H+ ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಸೂಚಿಸುವ ಉಸ್ತುವಾರಿ ವಹಿಸುತ್ತದೆ, ಅದರ ಆಮ್ಲೀಯ ಅಥವಾ ಮೂಲ ಪಾತ್ರವನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ.
ಈಜುಕೊಳದ ನೀರಿನ pH ಮೌಲ್ಯಗಳ ಪ್ರಮಾಣ


ಪೂಲ್ ವಾಟರ್ ಪಿಹೆಚ್ ಮಾಪನ ಮಾಪಕವು ಯಾವ ಮೌಲ್ಯಗಳನ್ನು ಒಳಗೊಂಡಿದೆ?
- pH ಮಾಪನ ಪ್ರಮಾಣವು 0 ರಿಂದ 14 ರವರೆಗಿನ ಮೌಲ್ಯಗಳನ್ನು ಒಳಗೊಂಡಿದೆ.
- ನಿರ್ದಿಷ್ಟವಾಗಿ 0 ಅತ್ಯಂತ ಆಮ್ಲೀಯವಾಗಿದೆ, 14 ಅತ್ಯಂತ ಮೂಲಭೂತವಾಗಿದೆ ಮತ್ತು ತಟಸ್ಥ pH ಅನ್ನು 7 ನಲ್ಲಿ ಇರಿಸುತ್ತದೆ.
- ಈ ಮಾಪನವನ್ನು ವಸ್ತುವಿನಲ್ಲಿರುವ ಉಚಿತ ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳ (H+) ಸಂಖ್ಯೆಯಿಂದ ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ.

ನಮಗೆ pH ಏಕೆ ಬೇಕು?
pH ಎಂಬುದು ಜಲೀಯ ದ್ರಾವಣದ ಆಮ್ಲೀಯತೆ ಅಥವಾ ಮೂಲಭೂತತೆಯನ್ನು ಸೂಚಿಸಲು ಬಳಸುವ ಅಳತೆಯಾಗಿದೆ. ಜಲೀಯ ದ್ರಾವಣವು ಆಮ್ಲ ಅಥವಾ ಬೇಸ್ ಆಗಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆಯೇ ಎಂಬುದು ಅದರ ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳ (H+) ಅಂಶವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.
ಆದಾಗ್ಯೂ, ರಾಸಾಯನಿಕವಾಗಿ ಶುದ್ಧ ಮತ್ತು ತಟಸ್ಥ ನೀರು ಸಹ ನೀರಿನ ಸ್ವಯಂ ವಿಘಟನೆಯಿಂದಾಗಿ ಕೆಲವು ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ಸ್ಟ್ಯಾಂಡರ್ಡ್ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ (750 mmHg ಮತ್ತು 25 ° C) ಸಮತೋಲನದಲ್ಲಿ, 1 L ಶುದ್ಧ ನೀರನ್ನು ಹೊಂದಿರುತ್ತದೆ ಎಂದು ತಿಳಿದಿದೆ ಚಿಟ್ಟೆ
y
ಚಿಟ್ಟೆ
ಅಯಾನುಗಳು, ಆದ್ದರಿಂದ, ಪ್ರಮಾಣಿತ ತಾಪಮಾನ ಮತ್ತು ಒತ್ತಡದಲ್ಲಿ (STP) ನೀರು 7 ರ pH ಅನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ನಮ್ಮ ಪೂಲ್ನ pH ಅನ್ನು ನಿಯಂತ್ರಿಸದಿದ್ದರೆ ಏನು ಮಾಡಬೇಕು

ಹೆಚ್ಚಿನ pH ಪೂಲ್ ಪರಿಣಾಮಗಳು ಮತ್ತು ನಿಮ್ಮ ಪೂಲ್ನಲ್ಲಿ ಹೆಚ್ಚಿನ pH ನ ಕಾರಣಗಳನ್ನು ತಿಳಿಯಿರಿ

ಪೂಲ್ನ pH ಅನ್ನು ಹೇಗೆ ಹೆಚ್ಚಿಸುವುದು ಮತ್ತು ಅದು ಕಡಿಮೆಯಾಗಿದ್ದರೆ ಏನಾಗುತ್ತದೆ

ಹೆಚ್ಚಿನ ಅಥವಾ ಕ್ಷಾರೀಯ ಪೂಲ್ pH ಅನ್ನು ಹೇಗೆ ಕಡಿಮೆ ಮಾಡುವುದು
pH ಜೊತೆಗೆ ಪೂಲ್ ನಿರ್ವಹಣೆಯನ್ನು ಹೇಗೆ ಮಾಡಬೇಕೆಂಬುದರ ಬಗ್ಗೆ ಮಾರ್ಗದರ್ಶಿಗಳು: ನೀರಿನ ಶುಚಿಗೊಳಿಸುವಿಕೆ ಮತ್ತು ಸೋಂಕುಗಳೆತ

ಪೂಲ್ ಅನ್ನು ಹೇಗೆ ಸ್ವಚ್ಛಗೊಳಿಸಬೇಕು ಎಂದು ತಿಳಿಯಲು ಉಪಯುಕ್ತ ಮಾರ್ಗದರ್ಶಿ

ಪರಿಪೂರ್ಣ ಸ್ಥಿತಿಯಲ್ಲಿ ನೀರಿನೊಂದಿಗೆ ಕೊಳವನ್ನು ನಿರ್ವಹಿಸಲು ಮಾರ್ಗದರ್ಶಿ
ಆಮ್ಲೀಯ, ತಟಸ್ಥ ಮತ್ತು ಕ್ಷಾರೀಯ pH ಮೌಲ್ಯಗಳು
pH ಮೌಲ್ಯಗಳ ಸ್ಕೇಲ್ನ ವರ್ಗೀಕರಣ
pH ಮೌಲ್ಯಗಳು ಯಾವುವು

pH ಪ್ರಮಾಣವು 1 ರಿಂದ 14 ರವರೆಗೆ ಹೋಗುತ್ತದೆ, pH 7 ತಟಸ್ಥ ಪರಿಹಾರವಾಗಿದೆ.
ಆದ್ದರಿಂದ, pH ಎಂಬುದು 0 (ಅತ್ಯಂತ ಆಮ್ಲೀಯ) ಮತ್ತು 14 (ಅತ್ಯಂತ ಕ್ಷಾರೀಯ) ಮೌಲ್ಯಗಳ ನಡುವೆ ಲಾಗರಿಥಮಿಕ್ ಪ್ರಮಾಣದಲ್ಲಿ ವ್ಯಕ್ತಪಡಿಸಲಾದ ಮೌಲ್ಯವಾಗಿದೆ ಎಂದು ಅದು ತಿರುಗುತ್ತದೆ; ನಡುವೆ ನಾವು ಮೌಲ್ಯ 7 ಅನ್ನು ತಟಸ್ಥವೆಂದು ಪಟ್ಟಿ ಮಾಡಿದ್ದೇವೆ.
pH ಪ್ರಮಾಣದ ಸಾರ್ವತ್ರಿಕ pH ಸೂಚಕ
ಒಂದು ವಸ್ತುವು ಆಮ್ಲೀಯ ಅಥವಾ ಕ್ಷಾರೀಯ pH ಮಟ್ಟವನ್ನು ಹೊಂದಿದೆ ಎಂದು ಇದರ ಅರ್ಥವೇನು?
ಆಮ್ಲಗಳು ಮತ್ತು ಬೇಸ್ಗಳು ಯಾವುವು?
ಆಮ್ಲಗಳು ಮತ್ತು ಬೇಸ್ಗಳು ಪ್ರಕೃತಿಯಲ್ಲಿ ಅಸ್ತಿತ್ವದಲ್ಲಿರುವ ಪದಾರ್ಥಗಳಾಗಿವೆ ಮತ್ತು ಅವುಗಳ pH ಮಟ್ಟದಿಂದ, ಅಂದರೆ ಅವುಗಳ ಆಮ್ಲೀಯತೆ ಅಥವಾ ಕ್ಷಾರೀಯತೆಯ ಮಟ್ಟದಿಂದ ಪ್ರತ್ಯೇಕಿಸಲ್ಪಡುತ್ತವೆ. ಪದಾರ್ಥಗಳು ಆಮ್ಲೀಯವೇ ಅಥವಾ ಕ್ಷಾರೀಯವೇ ಎಂಬುದನ್ನು ನಿರ್ಧರಿಸುವುದು ಆಮ್ಲೀಯತೆ ಅಥವಾ ಕ್ಷಾರೀಯತೆಯ ಮಟ್ಟವನ್ನು pH ಮಾಪಕದಿಂದ ಅಳೆಯಲಾಗುತ್ತದೆ ಮತ್ತು 0 ರಿಂದ 14 ರವರೆಗೆ (ಅತ್ಯಂತ ಕ್ಷಾರೀಯ) ವ್ಯಾಪ್ತಿಯಲ್ಲಿರುತ್ತದೆ. ಆದಾಗ್ಯೂ, ಎರಡೂ ಸಾಮಾನ್ಯವಾಗಿ ನಾಶಕಾರಿ, ಸಾಮಾನ್ಯವಾಗಿ ವಿಷಕಾರಿ ಪದಾರ್ಥಗಳಾಗಿವೆ. ಆದಾಗ್ಯೂ ಹಲವಾರು ಕೈಗಾರಿಕಾ ಮತ್ತು ಮಾನವ ಅನ್ವಯಗಳನ್ನು ಹೊಂದಿವೆ.
ಆಮ್ಲೀಯ ವಸ್ತುಗಳು ಯಾವುವು?
- ಆಮ್ಲ pH ಮಟ್ಟ: pH 7 ಕ್ಕಿಂತ ಕಡಿಮೆ
pH ಮೌಲ್ಯವು ಆಮ್ಲೀಯವಾಗಿದೆ ಎಂದು ಇದರ ಅರ್ಥವೇನು?
- ಒಂದು ವಸ್ತುವು ಆಮ್ಲೀಯವಾಗಿದೆ ಎಂದರೆ ಅದು H ನಲ್ಲಿ ಸಮೃದ್ಧವಾಗಿದೆ+ (ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳು): pH 7 ಕ್ಕಿಂತ ಹೆಚ್ಚು
- ಆದ್ದರಿಂದ, ಆಮ್ಲಗಳು pH 7 ಕ್ಕಿಂತ ಕಡಿಮೆ ಇರುವ ಪದಾರ್ಥಗಳಾಗಿವೆ. (7 ಕ್ಕೆ ಸಮಾನವಾದ ನೀರಿನ pH, ತಟಸ್ಥವೆಂದು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ), ಇದರ ರಸಾಯನಶಾಸ್ತ್ರವು ಸಾಮಾನ್ಯವಾಗಿ ನೀರನ್ನು ಸೇರಿಸುವಾಗ ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದ ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಅವು ಸಾಮಾನ್ಯವಾಗಿ ಪ್ರೋಟಾನ್ಗಳನ್ನು ಕಳೆದುಕೊಳ್ಳುವ ಮೂಲಕ ಇತರ ಪದಾರ್ಥಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ (H+).
ತಟಸ್ಥ ಪದಾರ್ಥಗಳು ಯಾವುವು?
- ತಟಸ್ಥ pH ಮೌಲ್ಯ: pH ಸಮಾನ 7-
pH ಮೌಲ್ಯವು ತಟಸ್ಥವಾಗಿದೆ ಎಂದು ಇದರ ಅರ್ಥವೇನು?
- pH ಎಂಬುದು ನೀರು ಎಷ್ಟು ಆಮ್ಲೀಯ/ಮೂಲಭೂತವಾಗಿದೆ ಎಂಬುದರ ಅಳತೆಯಾಗಿದೆ.
- ವ್ಯಾಪ್ತಿಯು 0 ರಿಂದ 14 ರವರೆಗೆ, 7 ತಟಸ್ಥವಾಗಿದೆ.
ಕ್ಷಾರೀಯ ವಸ್ತುಗಳು ಯಾವುವು?
- ಮೂಲ ಅಥವಾ ಕ್ಷಾರೀಯ pH ಹೊಂದಿರುವ ವಸ್ತುಗಳು: pH 7 ಕ್ಕಿಂತ ಹೆಚ್ಚು.
pH ಮೌಲ್ಯವು ಕ್ಷಾರೀಯವಾಗಿದ್ದರೆ ಇದರ ಅರ್ಥವೇನು?
- ಒಂದು ಪದಾರ್ಥವು ಕ್ಷಾರೀಯವಾಗಿದೆ ಎಂದರೆ ಅದು H ನಲ್ಲಿ ಕಳಪೆಯಾಗಿದೆ+ (ಅಥವಾ OH ಬೇಸ್ಗಳಲ್ಲಿ ಸಮೃದ್ಧವಾಗಿದೆ-, ಇದು H ಅನ್ನು ತಟಸ್ಥಗೊಳಿಸುತ್ತದೆ+).
- ಈ ಎಲ್ಲದಕ್ಕಾಗಿ, ಬೇಸ್ಗಳು, ಮತ್ತೊಂದೆಡೆ, 7 ಕ್ಕಿಂತ ಹೆಚ್ಚಿನ pH ಹೊಂದಿರುವ ಪದಾರ್ಥಗಳಾಗಿವೆ., ಇದು ಜಲೀಯ ದ್ರಾವಣಗಳಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿ ಹೈಡ್ರಾಕ್ಸಿಲ್ ಅಯಾನುಗಳನ್ನು ಒದಗಿಸುತ್ತದೆ (OH-) ಮಧ್ಯದಲ್ಲಿ. ಅವು ಶಕ್ತಿಯುತ ಆಕ್ಸಿಡೆಂಟ್ಗಳಾಗಿರುತ್ತವೆ, ಅಂದರೆ ಅವು ಸುತ್ತಮುತ್ತಲಿನ ಮಾಧ್ಯಮದಿಂದ ಪ್ರೋಟಾನ್ಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ.
pH ಮತ್ತು pOH ಮೌಲ್ಯಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸಗಳು

ಅವು ಹೇಗೆ ಸಂಬಂಧಿಸಿವೆ ಮತ್ತು ph ಮತ್ತು poh ಅಳತೆಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸವೇನು?
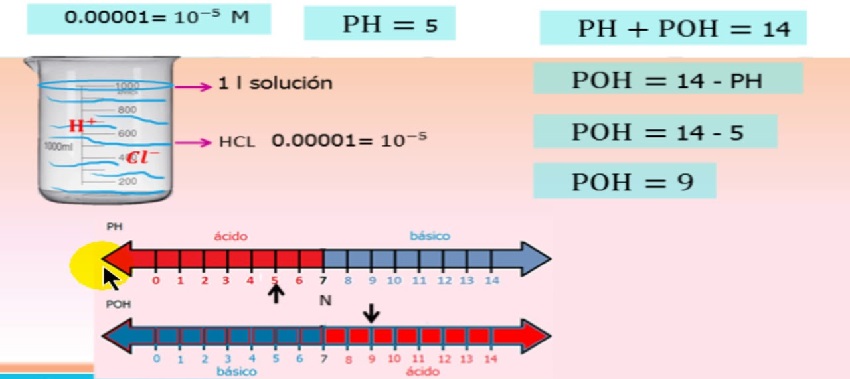
ಸಹಜವಾಗಿ, ಅಯಾನುಗಳ ಚಟುವಟಿಕೆಯು ಅಯಾನು ಸಾಂದ್ರತೆಯ ಮೇಲೆ ಅವಲಂಬಿತವಾಗಿರುತ್ತದೆ ಮತ್ತು ಇದನ್ನು ಸಮೀಕರಣದಲ್ಲಿ ವಿವರಿಸಲಾಗಿದೆ
pH/poH ಅಯಾನ್ ಚಟುವಟಿಕೆ ಸಮೀಕರಣ
ಎಲ್ಲಿ, - ಹೈಡ್ರೋಜನ್ ಅಯಾನು ಚಟುವಟಿಕೆ
- ಹೈಡ್ರೋಜನ್ ಅಯಾನಿನ ಚಟುವಟಿಕೆಯ ಗುಣಾಂಕ
- ಹೈಡ್ರೋಜನ್ ಅಯಾನು ಸಾಂದ್ರತೆ
ಚಟುವಟಿಕೆಯ ಗುಣಾಂಕವು ಅಯಾನು ಸಾಂದ್ರತೆಯ ಕಾರ್ಯವಾಗಿದೆ ಮತ್ತು ಪರಿಹಾರವು ಹೆಚ್ಚು ಹೆಚ್ಚು ದುರ್ಬಲಗೊಳ್ಳುವುದರಿಂದ 1 ಅನ್ನು ತಲುಪುತ್ತದೆ.
ದುರ್ಬಲಗೊಳಿಸುವ (ಆದರ್ಶ) ಪರಿಹಾರಗಳಿಗಾಗಿ, ದ್ರಾವಣದ ಪ್ರಮಾಣಿತ ಸ್ಥಿತಿಯು 1,00 M ಆಗಿರುತ್ತದೆ, ಆದ್ದರಿಂದ ಅದರ ಮೊಲಾರಿಟಿ ಅದರ ಚಟುವಟಿಕೆಗೆ ಸಮನಾಗಿರುತ್ತದೆ.
ಹೀಗಾಗಿ, ಆದರ್ಶ ಪರಿಹಾರಗಳನ್ನು ಊಹಿಸುವ ಹೆಚ್ಚಿನ ಸಮಸ್ಯೆಗಳಿಗೆ ನಾವು ಮೋಲಾರ್ ಸಾಂದ್ರತೆಯ ಬೇಸ್ 10 ಗೆ ಲಾಗರಿಥಮ್ ಅನ್ನು ಬಳಸಬಹುದು, ಚಟುವಟಿಕೆಯಲ್ಲ.
pH ಮತ್ತು pOH ನ ಮೌಲ್ಯದ ನಡುವಿನ ವ್ಯತ್ಯಾಸಗಳು

ಸಾಮಾನ್ಯ pH ಮೌಲ್ಯ ಏನು?
- ಒಂದು ರೀತಿಯಲ್ಲಿ, pH ಒಂದು ಅಳತೆಯಾಗಿದೆ ದ್ರಾವಣದ ಆಮ್ಲೀಯತೆ ಅಥವಾ ಕ್ಷಾರೀಯತೆಯ ಮಟ್ಟವನ್ನು ಸ್ಥಾಪಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ. "p" ಎಂದರೆ "ಸಂಭಾವ್ಯ", ಅದಕ್ಕಾಗಿಯೇ pH ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ: ಹೈಡ್ರೋಜನ್ ಸಾಮರ್ಥ್ಯ.
pOH ಮೌಲ್ಯ ಏನು?
- ನಿಮ್ಮ ಪಾಲಿಗೆ. pOH ಒಂದು ದ್ರಾವಣದಲ್ಲಿ ಹೈಡ್ರಾಕ್ಸಿಲ್ ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಯ ಅಳತೆಯಾಗಿದೆ. ಇದನ್ನು ಹೈಡ್ರಾಕ್ಸಿಲ್ ಅಯಾನ್ ಸಾಂದ್ರತೆಯ ಮೂಲ 10 ಋಣಾತ್ಮಕ ಲಾಗರಿಥಮ್ ಆಗಿ ವ್ಯಕ್ತಪಡಿಸಲಾಗುತ್ತದೆ ಮತ್ತು pH ಗಿಂತ ಭಿನ್ನವಾಗಿ, ದ್ರಾವಣದ ಕ್ಷಾರೀಯತೆಯ ಮಟ್ಟವನ್ನು ಅಳೆಯಲು ಬಳಸಲಾಗುತ್ತದೆ.

pH ಅಥವಾ pOH ಮೌಲ್ಯವನ್ನು ಹೇಗೆ ಲೆಕ್ಕ ಹಾಕಲಾಗುತ್ತದೆ?
ph ಪ್ರಮಾಣದ ಮೌಲ್ಯಗಳಿಗೆ ಸೂತ್ರ ಯಾವುದು?
- ಇದು ಈಗಾಗಲೇ ತಿಳಿದಿರುವಂತೆ, ವೈಜ್ಞಾನಿಕ ಕ್ಷೇತ್ರದಲ್ಲಿ, ದಿ pH ಅಳತೆಯಾಗಿದೆ de ಒಳಗಿನ ಅಯಾನುಗಳು de ಒಂದು ಪರಿಹಾರ. ನೀವು ಮಾಡಬೇಕಾಗಬಹುದು pH ಅನ್ನು ಲೆಕ್ಕಹಾಕಿ ಏಕಾಗ್ರತೆಯ ಆಧಾರದ ಮೇಲೆ. ಲೆಕ್ಕಾಚಾರ ಮಾಡಿ pH ನ ಸಮೀಕರಣವನ್ನು ಬಳಸುವುದು pH: pH = -ಲಾಗ್[H3O+].
pOH ಅನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡಲು ಸೂತ್ರ ಯಾವುದು?
- ಸಹ pOH (ಅಥವಾ OH ಸಂಭಾವ್ಯ) ಎಂಬುದು ಪರಿಹಾರದ ಮೂಲಭೂತತೆ ಅಥವಾ ಕ್ಷಾರೀಯತೆಯ ಅಳತೆಯಾಗಿದೆ. ಅಲ್ಲದೆ se pH ಬಳಸುತ್ತದೆ = – ಲಾಗ್ [H3O+ಹೈಡ್ರೋನಿಯಮ್ ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಅಳೆಯಲು [H3O+].

pH ಅಥವಾ pOH ಮೌಲ್ಯವನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡಲು ಪ್ರಮುಖ ಸಮೀಕರಣಗಳು
- pH=-ಲಾಗ್[H3O+]
- pOH=-ಲಾಗ್[OH−]
- [H3O+] = 10-pH
- [ಓಹ್-] = 10-pOH
- pH + pOH =ಪಿಕೆw = 14.00 25 °C ನಲ್ಲಿ.
pH ಮೌಲ್ಯಗಳ ಪ್ರಮಾಣ ಮತ್ತು pOH ನ ನಡುವಿನ ವ್ಯತ್ಯಾಸವೇನು?
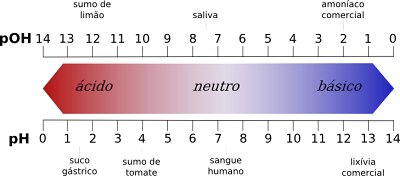
pH ಪ್ರಮಾಣದ ಮೌಲ್ಯಗಳ ನಡುವಿನ ಅಸಮಾನತೆಗಳು
- ಒಂದೆಡೆ, pH ಪ್ರಮಾಣವು 1 ರಿಂದ 6 ರವರೆಗೆ ಆಮ್ಲದ ಮೌಲ್ಯಗಳನ್ನು ನೀಡುತ್ತದೆ ಆದರೆ pOH ಪ್ರಮಾಣವು 8 ರಿಂದ 14 ರವರೆಗೆ ಆಮ್ಲ ಮೌಲ್ಯಗಳನ್ನು ನೀಡುತ್ತದೆ.
- ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, pH ಪ್ರಮಾಣವು 8 ರಿಂದ 14 ರವರೆಗಿನ ಮೂಲ ಮೌಲ್ಯಗಳನ್ನು ನೀಡುತ್ತದೆ, ಆದರೆ pOH ಪ್ರಮಾಣವು 1 ರಿಂದ 6 ರವರೆಗೆ ಮೂಲ ಮೌಲ್ಯಗಳನ್ನು ನೀಡುತ್ತದೆ.
ಅವುಗಳ ಮೌಲ್ಯಗಳೊಂದಿಗೆ ph ಮತ್ತು pOH ನ ಲಾಗರಿಥಮ್ ಸ್ಕೇಲ್ ಸಂಬಂಧ
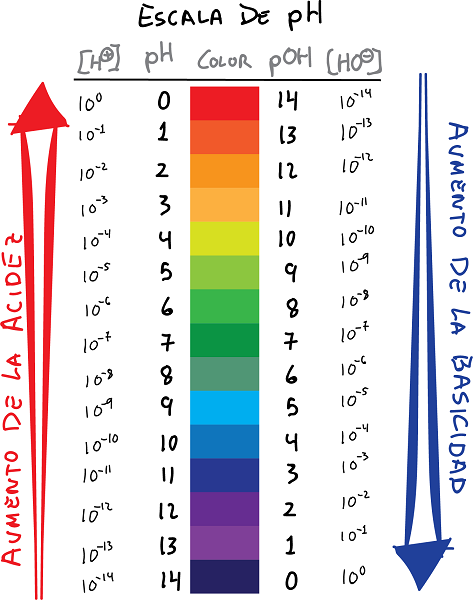
ಬಣ್ಣಗಳು ಮತ್ತು ಮೌಲ್ಯಗಳೊಂದಿಗೆ ph ಮತ್ತು pOH ಪ್ರಮಾಣದ ಸಂಪರ್ಕ
- pH H ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಯ ಲಾಗರಿಥಮ್ ಆಗಿದೆ+, ಚಿಹ್ನೆಯನ್ನು ಬದಲಾಯಿಸಲಾಗಿದೆ:
- ಅಂತೆಯೇ, ವ್ಯಾಖ್ಯಾನಿಸಿ pOH OH ಅಯಾನ್ ಸಾಂದ್ರತೆಯ ಲಾಗರಿಥಮ್ ಆಗಿ-, ಚಿಹ್ನೆಯನ್ನು ಬದಲಾಯಿಸುವುದರೊಂದಿಗೆ: ಕೆಳಗಿನ ಸಂಬಂಧವನ್ನು ನಡುವೆ ಸ್ಥಾಪಿಸಬಹುದು pH ಮತ್ತು pOH.
- ಮೂಲಭೂತವಾಗಿ, pH ಮೌಲ್ಯಗಳು ಹೈಡ್ರೋಜನ್ ಅಯಾನ್ ಸಾಂದ್ರತೆಯ ಋಣಾತ್ಮಕ ಲಾಗರಿಥಮ್ ಅನ್ನು ನೀಡುತ್ತವೆ, ಆದರೆ pOH ಮೌಲ್ಯವು ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನ್ ಸಾಂದ್ರತೆಯ ಋಣಾತ್ಮಕ ಲಾಗರಿಥಮ್ ಅನ್ನು ನೀಡುತ್ತದೆ.
pH ಮತ್ತು pOH ಮೌಲ್ಯಗಳ ಪ್ರಮಾಣದ ನಡುವಿನ ವ್ಯತ್ಯಾಸ
ph ಮೌಲ್ಯ ಕೋಷ್ಟಕ ಮತ್ತು pOH ಮೌಲ್ಯದ ನಡುವಿನ ವ್ಯತ್ಯಾಸಗಳು
ಅದರ ನಂತರ, ನಾವು ನಿಮಗೆ ಚಲನಚಿತ್ರವನ್ನು ಒದಗಿಸುತ್ತೇವೆ, ಅಲ್ಲಿ pH ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಅಳೆಯುತ್ತದೆ, ಆದರೆ pOH ಹೈಡ್ರಾಕ್ಸಿಲ್ ಅಯಾನುಗಳು ಅಥವಾ ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಅಳೆಯುತ್ತದೆ.


