
Skrá yfir innihald síðu
En Ok Pool Reform, í þessum hluta innan Sundlaugar með pH-gildi við munum meðhöndla munur á ph og poh í laugarvatnsgildum.
Hvert er pH í laug og hvernig ætti það að vera?

Hvað þýðir kjör pH fyrir sundlaugar (7,2-7,4)
Skammstöfunin pH stendur fyrir hugsanlegt vetni og er mælikvarði sem gefur til kynna sýrustig eða grunnstig vatns.
Svo, pH vísar til möguleika vetnis, gildi sem samsvarar styrk vetnisjóna í vatninu í lauginni þinni og er því stuðullinn sem gefur til kynna hversu sýrustig eða grunnstig vatnsins er. Þess vegna sér pH-gildið um að gefa til kynna styrk H+ jóna í vatninu, ákvarða súrt eða basískt eðli þess.
Kvarði pH-gilda í sundlaugarvatni


Hvaða gildi inniheldur pH mælikvarði laugarvatns?
- pH mælikvarðinn inniheldur gildi frá 0 til 14.
- Sérstaklega að vera 0 súrasta, 14 basískasta og setja hlutlausa pH við 7.
- Þessi mæling ræðst af fjölda frjálsra vetnisjóna (H+) í efninu.

Af hverju þurfum við pH?
pH er mælikvarði sem notaður er til að tilgreina sýrustig eða basleika vatnslausnar. Hvort vatnslausn hvarfast sem sýra eða basi fer eftir innihaldi vetnisjóna (H+).
Hins vegar inniheldur jafnvel efnafræðilega hreint og hlutlaust vatn nokkrar vetnisjónir vegna sjálfs sundrungar vatns.
Vitað er að við jafnvægi við staðlaðar aðstæður (750 mmHg og 25°C) inniheldur 1 L af hreinu vatni mól
y
mól
jónir, því hefur vatn við staðlað hitastig og þrýsting (STP) pH 7.
Hvað á að gera þegar pH laugarinnar okkar er EKKI stjórnað

Þekkja afleiðingar há pH laug og orsakir hás pH í lauginni þinni

Hvernig á að hækka pH laugarinnar og hvað gerist ef það er lágt

Hvernig á að lækka hátt eða basískt pH í lauginni
Leiðbeiningar um hvernig á að gera sundlaugarviðhald auk pH: vatnsþrif og sótthreinsun

Gagnleg leiðarvísir til að vita hvernig á að þrífa sundlaug

Leiðbeiningar um að viðhalda laug með vatni í fullkomnu ástandi
Súrt, hlutlaust og basískt pH gildi
Flokkun á kvarða pH-gilda
Hver eru pH gildin

pH kvarðinn fer frá 1 til 14, þar sem pH 7 er hlutlaus lausn.
Svo kemur í ljós að pH er gildi sem er gefið upp á logaritmískum kvarða á milli gildanna 0 (mjög súrt) og 14 (mjög basískt); Þar á milli finnum við gildið 7 flokkað sem hlutlaust.
Alhliða pH mælikvarði pH mælikvarða
Hvað þýðir það að efni hafi súrt eða basískt pH gildi?
Hvað eru sýrur og basar?
Sýrur og basar eru efni sem eru til í náttúrunni og eru aðgreind með pH-gildi, það er sýrustigi eða basastigi. Ákvörðun á því hvort efni eru súr eða basísk ræðst af sýrustigi eða basastigi sem mælt er í gegnum pH kvarðann og er á bilinu 0 (mjög súrt til 14 (mjög basískt). Bæði eru þó yfirleitt ætandi, oft eitruð efni sem engu að síður hafa fjölmörg iðnaðar- og mannvirkjanotkun.
Hvað eru súr efni?
- Sýru pH gildi: pH minna en 7
Hvað þýðir það að pH gildið sé súrt?
- Að efni sé súrt þýðir að það er ríkt af H+ (vetnisjónir): pH hærra en 7
- Þess vegna, Sýrur eru efni með pH minna en 7. (pH vatns jafnt og 7, talið hlutlaust), en efnafræði þess inniheldur venjulega mikið magn af vetnisjónum þegar vatni er bætt við. Þeir bregðast venjulega við öðrum efnum með því að tapa róteindum (H+).
Hvað eru hlutlaus efni?
- Hlutlaust pH gildi: pH jafnt og 7-
Hvað þýðir það að pH gildið sé hlutlaust?
- pH er mælikvarði á hversu súrt/basískt vatnið er.
- Sviðið er frá 0 til 14, þar sem 7 er hlutlaust.
Hvað eru basísk efni?
- Efni með basa eða basískt pH: pH hærra en 7.
Hvað þýðir það þegar pH gildið er basískt?
- Að efni sé basískt þýðir að það er lélegt í H+ (eða ríkur af OH basa-, sem gera H+).
- Fyrir allt þetta, Basar eru aftur á móti efni með pH hærra en 7., sem í vatnslausnum gefur venjulega hýdroxýljónir (OH-) í miðjunni. Þeir hafa tilhneigingu til að vera öflug oxunarefni, það er að segja að þeir hvarfast við róteindir úr nærliggjandi miðli.
Mismunur á pH og pOH gildi

Hvernig tengjast þau og hver er munurinn á ph og poh mælingum?
Virkni jónanna fer auðvitað eftir jónastyrknum og er því lýst í jöfnunni
pH/poH jónavirknijafna
hvar, – vetnisjónavirkni
– virknistuðull vetnisjónarinnar
– styrkur vetnisjóna
Virknistuðullinn er fall af jónastyrk og nálgast 1 eftir því sem lausnin verður meira og meira þynnt.
Fyrir þynntar (tilvalin) lausnir er staðlað ástand uppleysts efnisins 1,00 M, þannig að mólstyrkur þess jafngildir virkni þess.
Þannig að fyrir flest vandamál sem gera ráð fyrir hugsjónalausnum getum við notað lógaritma við grunn 10 mólstyrksins, ekki virknina.
Mismunur á því hvað er gildi pH og pOH

Hvert er eðlilegt pH gildi?
- Á vissan hátt er pH mælikvarði sem notað til að ákvarða sýrustig eða basastig lausnar. „P“ stendur fyrir „möguleika“, þess vegna er pH kallað: möguleiki vetnis.
Hvað er pOH gildið?
- Fyrir þitt leyti. pOH er mælikvarði á styrk hýdroxýljóna í lausn. Það er gefið upp sem basa 10 neikvæður logaritmi hýdroxýljónastyrksins og, ólíkt pH, er hann notaður til að mæla basastig lausnar.

Hvernig er pH eða pOH gildið reiknað út?
Hver er formúlan fyrir ph-kvarðagildi?
- Eins og það er þegar vitað, á vísindasviðinu, er pH er mælikvarðinn de jónirnar inni de lausn. Þú gætir þurft að reikna pH byggt á einbeitingu. Reiknaðu út pH Með því að nota jöfnuna af pH: pH = -log[H3O+].
Hver er formúlan til að reikna út pOH?
- Einnig, the pOH (eða OH möguleiki) er mælikvarði á grunnleika eða basaleika lausnar. Einnig se notar pH = – log [H3O+] til að mæla styrk hýdróníumjóna [H3O+].

Lykiljöfnur til að reikna út pH eða pOH gildi
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [Ó-] = 10-pOH
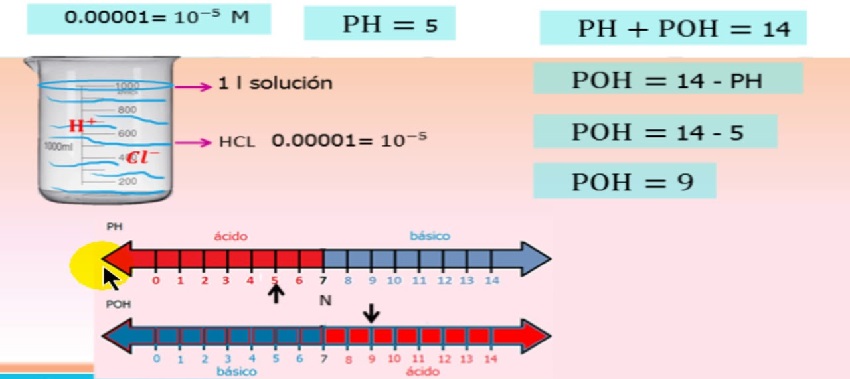
- pH + pOH =pKw = 14.00 við 25 °C.
Hver er munurinn á kvarða pH-gilda og pOH?
Ójöfnuður milli gilda pH kvarðans
- Annars vegar gefur pH kvarðinn sýrugildi frá 1 til 6 á meðan pOH kvarðinn gefur sýrugildi frá 8 til 14.
- Aftur á móti gefur pH kvarðinn grunngildi frá 8 til 14, en pOH kvarðinn gefur grunngildi frá 1 til 6.
Logaritmakvarðasamband ph og pOH við gildi þeirra
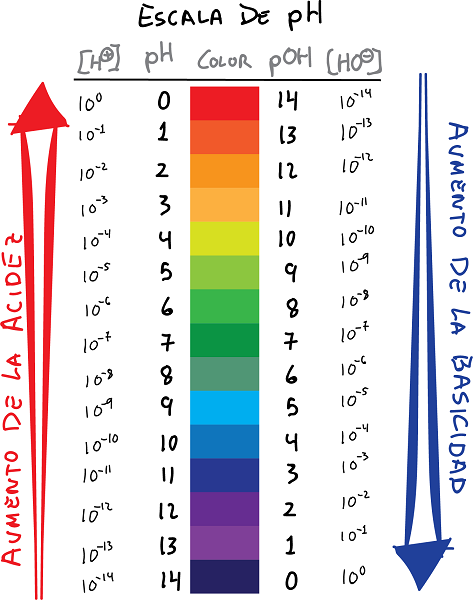
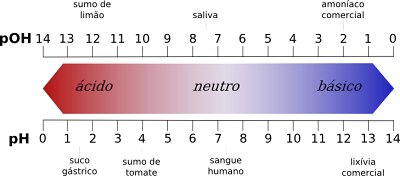
ph og pOH kvarðatenging við liti og gildi
- pH er logaritmi styrks H jóna+, með merkinu breytt:
- Á sama hátt, skilgreina pOH sem logaritmi OH jónastyrksins-, með merkinu breytt: Eftirfarandi samband má koma á milli pH og pOH.
- Í grundvallaratriðum gefa pH gildin neikvæðan logaritma vetnisjónastyrksins, en pOH gildið gefur neikvæðan logaritma hýdroxíðjónastyrksins.
Mismunur á kvarða pH og pOH gildi
Misræmi á milli ph gildi töflu og pOH gildi
Eftir það gefum við þér kvikmynd þar sem þú getur séð að pH mælir styrk vetnisjóna, en pOH mælir styrk hýdroxýlanjóna eða hýdroxíðjóna.


