
Az oldal tartalmának mutatója
En Ok medence reform, ebben a részben a pH-szintű úszómedencék kezeljük a különbség a ph és a poh között a medencevíz értékekben.
Mi a pH a medencében, és milyennek kell lennie?

Mit jelent az ideális pH úszómedencéknél (7,2-7,4)
A pH mozaikszó a potenciális hidrogént jelenti, és a víz savasságát vagy bázikusságát jelzi.
Akkor, A pH a hidrogén potenciáljára utal, ez az érték a medencédben lévő vízben lévő hidrogénionok koncentrációjának felel meg, és ezért a víz savasságának vagy bázikusságának mértékét jelző együttható. Ezért a pH határozza meg a vízben lévő H+ ionok koncentrációját, meghatározza annak savas vagy bázikus jellegét.
Az uszodavíz pH-értékeinek skálája


Milyen értékeket tartalmaz a medencevíz pH-mérőskála?
- A pH mérési skála 0 és 14 közötti értékeket tartalmaz.
- Főleg, hogy 0 a legsavasabb, 14 a legbázikusabb, és a semleges pH-t 7-re állítja.
- Ezt a mérést az anyagban lévő szabad hidrogénionok (H+) száma határozza meg.

Miért van szükségünk pH-ra?
A pH a vizes oldat savasságának vagy bázikusságának meghatározására szolgáló mérték. Az, hogy egy vizes oldat savként vagy bázisként reagál, a hidrogénion-tartalmától (H+) függ.
Azonban még a kémiailag tiszta és semleges víz is tartalmaz néhány hidrogéniont a víz öndisszociációja miatt.
Ismeretes, hogy normál körülmények között egyensúlyban (750 Hgmm és 25°C) 1 liter tiszta víz tartalmaz. mol
y
mol
ionok, ezért a víz standard hőmérsékleten és nyomáson (STP) pH-ja 7.
Mi a teendő, ha medencénk pH-ja NINCS szabályozott

Ismerje meg a magas pH-jú medence következményeit és a magas pH-érték okait a medencében

Hogyan növelhető a medence pH-ja, és mi történik, ha alacsony

Hogyan csökkenthető a magas vagy lúgos medence pH-ja
Útmutató a medence karbantartásához a pH mellett: víztisztítás és fertőtlenítés
Savas, semleges és lúgos pH-értékek
A pH-értékek skála osztályozása
Mik a pH értékek

A pH-skála 1-től 14-ig terjed, a pH 7 semleges oldat.
Tehát kiderül, hogy a pH egy olyan érték, amelyet logaritmikus skálán fejeznek ki a 0 (rendkívül savas) és 14 (nagyon lúgos) értékek között; Között a 7-es értéket semlegesnek katalógusban találjuk.
pH skála univerzális pH indikátor
Mit jelent az, hogy egy anyag pH-értéke savas vagy lúgos?
Mik azok a savak és bázisok?
A savak és a bázisok a természetben létező anyagok, amelyeket pH-értékük, azaz savasságuk vagy lúgosságuk mértéke különböztet meg. Annak meghatározását, hogy az anyagok savasak vagy lúgosak-e, a pH-skálán mért savasság vagy lúgosság mértéke szabályozza, és 0-tól (extrém savas és 14-ig (nagyon lúgos)) terjed. Mindazonáltal mindkettő általában maró, gyakran mérgező anyag. ennek ellenére számos ipari és emberi felhasználási területük van.
Mik azok a savas anyagok?
- Savas pH-szint: pH kisebb, mint 7
Mit jelent az, hogy a pH-érték savas?
- Az, hogy egy anyag savas, azt jelenti, hogy gazdag H-ban+ (hidrogénionok): pH 7-nél nagyobb
- Ennélfogva, A savak olyan anyagok, amelyek pH-ja 7-nél kisebb. (a víz pH-ja 7, semlegesnek tekinthető), amelynek kémiája általában nagy mennyiségű hidrogéniont tartalmaz víz hozzáadásakor. Általában más anyagokkal reagálnak protonok elvesztésével (H+).
Mik azok a semleges anyagok?
- Semleges pH-érték: pH egyenlő 7-
Mit jelent az, hogy a pH-érték semleges?
- A pH annak mértéke, hogy mennyire savas/lúgos a víz.
- A tartomány 0 és 14 között van, a 7 pedig semleges.
Mik azok a lúgos anyagok?
- Bázikus vagy lúgos pH-jú anyagok: pH 7-nél nagyobb.
Mit jelent, ha a pH-érték lúgos?
- Az, hogy egy anyag lúgos, azt jelenti, hogy H-szegény+ (vagy OH-bázisokban gazdag-, amelyek semlegesítik a H+).
- Mindehhez, A bázisok viszont 7-nél nagyobb pH-jú anyagok., amelyek vizes oldatokban általában hidroxil-ionokat (OH-) középen. Általában erős oxidálószerek, azaz reagálnak a környező közegből származó protonokkal.
A pH és a pOH értékek közötti különbségek

Hogyan kapcsolódnak egymáshoz, és mi a különbség a ph és a poh mérések között?
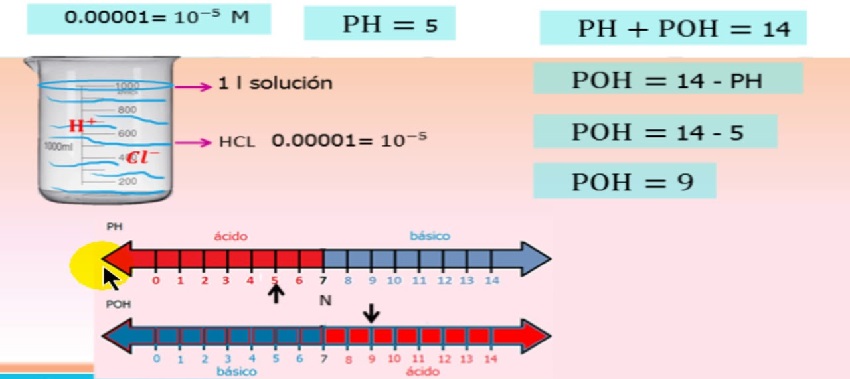
Természetesen az ionok aktivitása függ az ionkoncentrációtól és ezt az egyenlet írja le
pH/poH ionaktivitás egyenlet
ahol, – hidrogénion aktivitás
– a hidrogénion aktivitási együtthatója
– hidrogénion koncentráció
Az aktivitási együttható az ionkoncentráció függvénye, és az oldat egyre hígabbá válásával megközelíti az 1-et.
Híg (ideális) oldatok esetén az oldott anyag standard állapota 1,00 M, tehát molaritása megegyezik az aktivitásával.
Így a legtöbb olyan probléma esetében, amely ideális megoldást feltételez, a moláris koncentráció 10-es bázisának logaritmusát használhatjuk, nem az aktivitást.
A pH és a pOH értéke közötti különbségek

Mi a normál pH-érték?
- A pH bizonyos értelemben annak mértéke az oldat savasságának vagy lúgosságának meghatározására szolgál. A „p” a „potenciál” rövidítése, ezért a pH-t a hidrogén potenciáljának nevezik.
Mi a pOH értéke?
- A maga részéről. A pOH a hidroxil-ionok koncentrációjának mértéke az oldatban. Ezt a hidroxil-ion-koncentráció 10-es negatív logaritmusaként fejezzük ki, és a pH-tól eltérően az oldat lúgossági szintjének mérésére szolgál.

Hogyan számítják ki a pH vagy pOH értéket?
Mi a ph skálaértékek képlete?
- Mint az már ismert, a tudományos területen a pH az a mérték de a benne lévő ionok de egy megoldás. Lehet, hogy muszáj lesz számítsuk ki a pH-t koncentráció alapján. Számítsa ki a pH Az egyenlet felhasználásával pH: pH = -log [H3O+].
Mi a képlet a pOH kiszámításához?
- Továbbá, a pOH (vagy OH potenciál) az oldat bázikusságának vagy lúgosságának mértéke. Is se a pH = – log [H3O+] a hidrogénionok koncentrációjának mérésére [H3O+].

Kulcs egyenletek a pH vagy pOH érték kiszámításához
- pH=-log[H3O+]
- pOH=-log[OH-]
- [H3O+] = 10-pH
- [ó-] = 10-pOH
- pH + pOH =pKw = 14.00 25 °C-on.
Mi a különbség a pH-érték skála és a pOH-érték között?
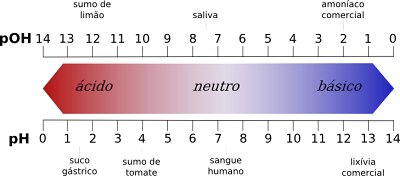
A pH-skála értékei közötti egyenlőtlenségek
- Egyrészt a pH-skála 1-től 6-ig, míg a pOH-skála 8-tól 14-ig terjedő savértékeket ad.
- Ezzel szemben a pH-skála 8-tól 14-ig, míg a pOH-skála 1-től 6-ig terjedő alapértékeket ad.
A ph és a pOH logaritmusskála kapcsolata értékeivel
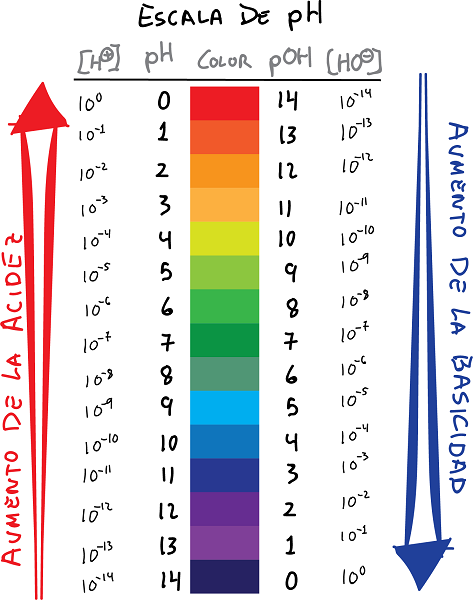
ph és pOH skála kapcsolat színekkel és értékekkel
- pH a H-ionok koncentrációjának logaritmusa+, megváltozott előjellel:
- Hasonlóképpen határozza meg pOH mint az OH ionkoncentráció logaritmusa-, megváltozott előjellel: A következő kapcsolat állapítható meg a pH és pOH.
- A pH-értékek alapvetően a hidrogénion-koncentráció negatív logaritmusát, míg a pOH-érték a hidroxidion-koncentráció negatív logaritmusát adják meg.
A pH és a pOH értékek skála közötti különbség
Eltérések a ph érték táblázat és a pOH érték között
Ezek után egy filmet adunk, ahol láthatod, hogy a pH a hidrogénionok, míg a pOH a hidroxil-anionok vagy hidroxidionok koncentrációját méri.




