
Yndeks fan side ynhâld
En Ok Pool Reform, yn dizze seksje binnen de pH nivo swimbaden wy sille behannelje de ferskil tusken ph en poh yn swimwetterwearden.
Wat is de pH yn in swimbad en hoe moatte har nivo's wêze?

Wat betsjut ideale pH foar swimbaden (7,2-7,4)
It akronym pH stiet foar potinsjele wetterstof en is in maatregel dy't de acidity of basicity fan wetter oanjout.
Dus, pH ferwiist nei it potinsjeel fan wetterstof, in wearde dy't oerienkomt mei de konsintraasje fan wetterstofionen yn it wetter yn jo swimbad en is dêrom de koëffisjint dy't de graad fan aciditeit of basiciteit fan it wetter oanjout. Dêrom is de pH ferantwurdlik foar it oanjaan fan de konsintraasje fan H + -ionen yn it wetter, it bepalen fan har soere of basale karakter.
Skaal fan pH-wearden fan swimbadwetter


Hokker wearden omfettet de pH-mjittingskaal fan it swimbadwetter?
- De pH-mjittingskaal omfettet wearden fan 0 oant 14.
- Benammen 0 de meast soer, 14 de meast basale en it pleatsen fan de neutrale pH op 7.
- Dizze mjitting wurdt bepaald troch it oantal frije wetterstofionen (H+) yn 'e stof.

Wêrom hawwe wy pH nedich?
pH is in maatregel dy't brûkt wurdt om de aciditeit of basiciteit fan in wetterige oplossing oan te jaan. Oft in wetterige oplossing reagearret as in soer of in base hinget ôf fan de ynhâld fan wetterstofionen (H+).
Sels chemysk suver en neutraal wetter befettet lykwols wat wetterstofionen troch sels-dissoziaasje fan wetter.
It is bekend dat by lykwicht ûnder standertbetingsten (750 mmHg en 25 °C), 1 L suver wetter befettet sêft
y
sêft
ionen hat dêrom wetter by standert temperatuer en druk (STP) in pH fan 7.
Wat te dwaan as de pH fan ús swimbad NET regele is

Ken de konsekwinsjes fan hege pH-pool en de oarsaken fan in hege pH yn jo swimbad

Hoe kinne jo de pH fan it swimbad ferheegje en wat bart as it leech is

Hoe kinne jo in hege of alkaline pH fan in swimbad ferleegje
Hantliedingen oer hoe't jo swimbadûnderhâld dwaan neist pH: wetterreiniging en desinfeksje

Nuttige hantlieding om te witten hoe't jo in swimbad skjinmeitsje

Gids foar it behâld fan in swimbad mei wetter yn perfekte steat
Soere, neutrale en alkaline pH-wearden
Klassifikaasje fan 'e skaal fan pH-wearden
Wat binne de pH-wearden

De pH-skaal giet fan 1 oant 14, wêrby't pH 7 in neutrale oplossing is.
Dat, it docht bliken dat pH in wearde is dy't wurdt útdrukt op in logaritmyske skaal tusken de wearden 0 (ekstreem soer) en 14 (ekstreem alkaline); Dêrtusken fine wy de wearde 7 katalogisearre as neutraal.
pH-skaal universele pH-yndikator
Wat betsjut it dat in stof in soere of alkaline pH-nivo hat?
Wat binne soeren en basen?
Soeren en basen binne stoffen dy't yn 'e natuer besteane en wurde ûnderskieden troch har pH-nivo, dat is troch har graad fan aciditeit of alkaliniteit. De bepaling oft stoffen soer of alkalisk binne wurdt regele troch de graad fan aciditeit of alkaliniteit mjitten troch de pH-skaal en rint fan 0 (ekstreem soer oant 14 (ekstreem alkaline). Beide binne lykwols meastentiids korrosive, faak giftige stoffen, wat hawwe lykwols in protte yndustriële en minsklike tapassingen.
Wat binne soere stoffen?
- Acid pH-nivo: pH minder dan 7
Wat betsjut it dat de pH-wearde soer is?
- Dat in stof soer is betsjut dat it ryk is oan H+ (hydrogen-ionen): pH grutter dan 7
- Dêrom, Soeren binne stoffen mei in pH minder dan 7. (pH fan wetter lyk oan 7, as neutraal beskôge), wêrfan de skiekunde gewoanlik grutte hoemannichten wetterstofionen befettet by it tafoegjen fan wetter. Se reagearje normaal mei oare stoffen troch protoanen te ferliezen (H+).
Wat binne neutrale stoffen?
- Neutrale pH-wearde: pH lyk oan 7-
Wat betsjut it dat de pH-wearde neutraal is?
- pH is in mjitting fan hoe soer/basis it wetter is.
- It berik is fan 0 oant 14, mei 7 neutraal.
Wat binne alkaline stoffen?
- Substanzen mei base of alkaline pH: pH grutter dan 7.
Wat betsjut it as de pH-wearde alkaline is?
- Dat in stof alkaline is, betsjut dat it min is yn H+ (of ryk oan OH-basen-, dy't de H+).
- Foar dit alles, Basen, oan 'e oare kant, binne stoffen mei in pH grutter dan 7., dy't yn wetterige oplossingen gewoanlik hydroxylionen leverje (OH-) yn it midden. Se binne meast krêftige oksidanten, dat is, se reagearje mei protoanen út it omlizzende medium.
Ferskillen tusken pH en pOH wearden

Hoe binne se besibbe en wat binne de ferskillen tusken ph- en poh-mjittingen?
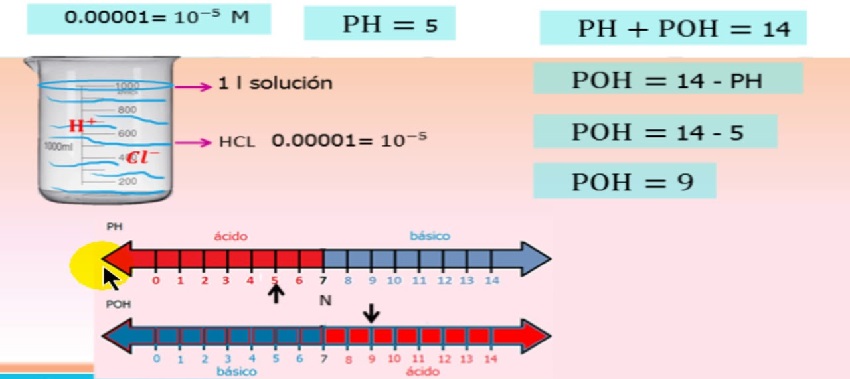
Fansels hinget de aktiviteit fan 'e ioanen ôf fan' e ionkonsintraasje en dit wurdt beskreaun yn 'e fergeliking
pH / poH ionaktiviteit fergeliking
wêr, - wetterstof ion aktiviteit
- aktiviteitskoëffisjint fan it wetterstofion
- konsintraasje fan wetterstofion
De aktiviteitskoëffisjint is in funksje fan ionkonsintraasje en benaderet 1 as de oplossing mear en mear verdund wurdt.
Foar verdunde (ideale) oplossingen is de standert tastân fan 'e solute 1,00 M, sadat de molariteit syn aktiviteit is.
Sa kinne wy foar de measte problemen dy't ideale oplossingen oannimme, de logaritme brûke oan 'e basis 10 fan' e molêre konsintraasje, net de aktiviteit.
Ferskillen tusken wat is de wearde fan pH en pOH

Wat is de normale pH-wearde?
- Op in manier is pH in maatregel dat brûkt om it nivo fan aciditeit of alkaliniteit fan in oplossing te bepalen. De "p" stiet foar "potential", en dêrom wurdt pH neamd: potinsjeel fan wetterstof.
Wat is de pOH wearde?
- Foar dyn part. pOH is in mjitting fan de konsintraasje fan hydroxyl-ionen yn in oplossing. It wurdt útdrukt as de basis 10 negative logaritme fan 'e hydroxylionkonsintraasje en, yn tsjinstelling ta pH, wurdt it brûkt om it alkaliniteitnivo fan in oplossing te mjitten.

Hoe wurdt de pH of pOH wearde berekkene?
Wat is de formule foar ph-skaalwearden?
- Sa't it is al bekend, op it wittenskiplik mêd, de pH is de maat de de ionen binnen de in oplossing. Jo kinne moatte berekkenje pH basearre op konsintraasje. Berekkenje de pH Mei help fan de fergeliking fan pH: pH = -log[H3O+].
Wat is de formule om pOH te berekkenjen?
- Ek de pOH (of OH-potinsjeel) is in mjitting fan 'e basiciteit of alkaliniteit fan in oplossing. Ek se brûkt de pH = - log [H3O+] om de konsintraasje fan hydroniumionen te mjitten [H3O+].

Key Fergelikingen om de pH- of pOH-wearde te berekkenjen
- pH=-log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [oant-] = 10-pOH
- pH + pOH =pKw = 14.00 by 25 °C.
Wat is it ferskil tusken de skaal fan pH-wearden en dy fan pOH?
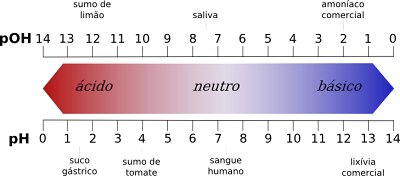
Ungelikens tusken de wearden fan 'e pH-skaal
- Oan 'e iene kant jout de pH-skaal soere wearden fan 1 oant 6, wylst de pOH-skaal soerwearden jout fan 8 oant 14.
- Oarsom jout de pH-skaal basiswearden fan 8 oant 14, wylst de pOH-skaal basiswearden jout fan 1 oant 6.
Logaritme skaal relaasje fan ph en pOH mei harren wearden
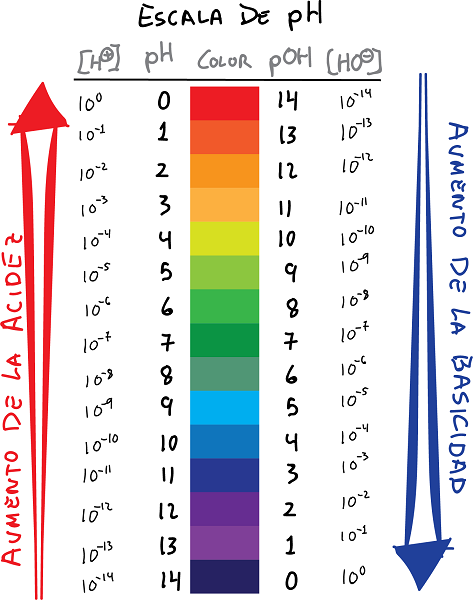
ph- en pOH-skaalferbining mei kleuren en wearden
- pH is de logaritme fan de konsintraasje fan H-ionen+, mei it teken feroare:
- Lykas, definiearje pOH as de logaritme fan 'e OH-ionkonsintraasje-, mei it teken feroare: De folgjende relaasje kin fêststeld wurde tusken de pH en de pOH.
- Yn prinsipe jouwe de pH-wearden de negative logaritme fan 'e konsintraasje fan wetterstofion, wylst de pOH-wearde de negative logaritme fan' e hydroxide-ionkonsintraasje jout.
Ferskil tusken de skaal fan pH en pOH wearden
Diskrepânsjes tusken de ph wearde tabel en pOH wearde
Dêrnei jouwe wy jo in film wêr't jo kinne sjen dat pH de konsintraasjes fan wetterstofionen mjit, wylst pOH de konsintraasjes fan hydroxylanionen of hydroxide-ionen mjit.


