
Orriaren aurkibidea
En Ados Igerilekuen Erreforma, atal honetan pH-mailako igerilekuak tratatuko dugu ph eta poh-ren arteko aldea igerilekuko uraren balioetan.
Zein da igerileku bateko pH-a eta nola izan behar du bere mailak?

Zer esan nahi du pH idealak igerilekuetarako (7,2-7,4)
pH akronimoak hidrogeno potentziala adierazten du eta uraren azidotasuna edo basikotasuna adierazten duen neurria da.
Ondoren, pH-ak hidrogenoaren potentzialari egiten dio erreferentzia, zure igerilekuko uretan dagoen hidrogeno ioien kontzentrazioari dagokion balioa eta, beraz, uraren azidotasun edo basikotasun maila adierazten duen koefizientea da. Hori dela eta, pH-a uraren H + ioien kontzentrazioak bere izaera azidoa edo basikoa zehazten duela adierazteko arduraduna da.
Igerilekuko uraren pH balioen eskala


Zein balio hartzen ditu igerilekuko uraren pH-a neurtzeko eskalak?
- pH neurtzeko eskalak 0 eta 14 bitarteko balioak biltzen ditu.
- Batez ere 0 azidoena izanik, 14 oinarrizkoena eta pH Neutroa 7an jarriz.
- Neurketa hau substantzian dagoen hidrogeno ioi askeen (H+) kopuruaren arabera zehazten da.

Zergatik behar dugu pH-a?
pH-a ur-disoluzio baten azidotasuna edo basikotasuna zehazteko erabiltzen den neurria da. Ur-disoluzio batek azido edo base gisa erreakzionatzen duen ala ez, hidrogeno ioien (H+) edukiaren araberakoa da.
Hala ere, ur kimikoki puruak eta neutroak ere hidrogeno ioi batzuk ditu uraren auto-disoziazioaren ondorioz.
Jakina da orekan baldintza estandarretan (750 mmHg eta 25°C), 1 L ur puruak dituela. mol
y
mol
ioiak, beraz, tenperatura eta presio estandarrean (STP) urak 7ko pH-a du.
Zer egin gure igerilekuko pH-a erregulatuta EZ dagoenean

Ezagutu pH altuko igerilekuaren ondorioak eta zure igerilekuan pH altuaren arrazoiak

Nola igo igerilekuaren pHa eta zer gertatzen den baxua bada

Nola jaitsi pH altua edo alkalinoa
pHaz gain igerilekuen mantentze-lanak egiteko gidak: ura garbitzea eta desinfekzioa

Gida erabilgarria igerilekua nola garbitu jakiteko

Ura egoera ezin hobean duen igerilekua mantentzeko gida
pH azido, neutro eta alkalinoaren balioak
pH Balioen Eskalaren sailkapena
Zeintzuk dira pH-aren balioak

pH eskala 1etik 14ra doa, pH 7 disoluzio neutroa izanik.
Beraz, pH-a 0 (oso azidoa) eta 14 (oso alkalinoa) balioen artean eskala logaritmikoan adierazten den balio bat da; Tartean 7 balioa neutro gisa katalogatuta aurkitzen dugu.
pH eskala pH adierazle unibertsala
Zer esan nahi du substantzia batek pH maila azidoa edo alkalinoa duela?
Zer dira azidoak eta baseak?
Azidoak eta baseak naturan dauden substantziak dira eta pH mailagatik bereizten dira, hau da, azidotasun edo alkalinitate mailagatik. Substantziak azidoak edo alkalinoak diren zehaztea pH eskalaren bidez neurtutako azidotasun edo alkalinitate-mailaren araberakoa da eta 0tik (oso azidoa eta 14ra (oso alkalinoa). Biak, ordea, substantzia korrosiboak izan ohi dira, askotan toxikoak, zeinak. hala ere, industria eta giza aplikazio ugari dituzte.
Zer dira substantzia azidoak?
- pH azidoaren maila: pH 7 baino txikiagoa
Zer esan nahi du pH balioa azidoa dela?
- Substantzia azidoa izateak esan nahi du H-tan aberatsa dela+ (hidrogeno ioiak): pH 7 baino handiagoa
- Horregatik, Azidoak 7 baino pH txikiagoa duten substantziak dira. (uraren pH berdina 7, neutrotzat jotzen da), zeinaren kimikak normalean hidrogeno ioi kopuru handiak ditu ura gehitzean. Normalean beste substantziekin erreakzionatzen dute protoiak galduz (H+).
Zer dira substantzia neutroak?
- pH neutroaren balio: pH 7-ren berdina
Zer esan nahi du pH balioa neutroa dela?
- pH-a ura zein azido/basikoa den neurtzen du.
- Tartea 0tik 14ra da, 7 neutroa izanik.
Zer dira substantzia alkalinoak?
- pH base edo alkalinoa duten substantziak: pH 7 baino handiagoa.
Zer esan nahi du pH balioa alkalinoa denean?
- Substantzia alkalinoa izateak esan nahi du H-tan pobrea dela+ (edo OH oinarrietan aberatsa-, H neutralizatzen dutenak+).
- Horregatik guztiagatik, Baseak, berriz, 7 baino pH handiagoa duten substantziak dira., ur-disoluzioetan hidroxilo ioiak (OH-) erdian. Oxidatzaile indartsuak izan ohi dira, hau da, inguruko medioko protoiekin erreakzionatzen dute.
pH eta pOH balioen arteko aldeak

Nola erlazionatzen dira eta zein dira ph eta poh neurketen arteko aldeak?
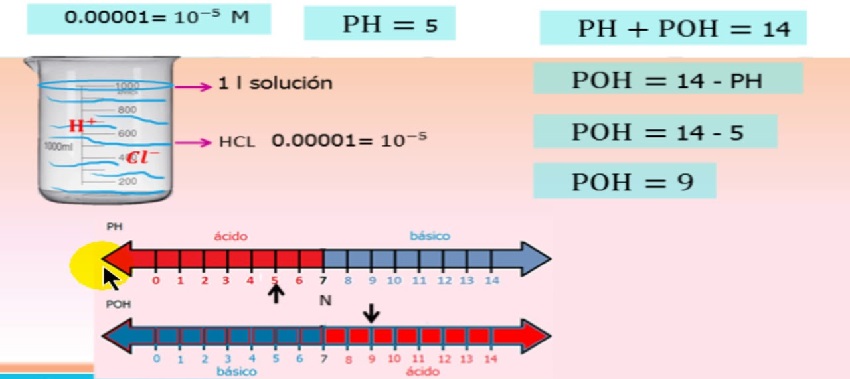
Noski, ioien jarduera ioien kontzentrazioaren araberakoa da eta hori ekuazioan deskribatzen da
pH/poH ioien jardueraren ekuazioa
non, – Hidrogeno ioien jarduera
– Hidrogeno ioiaren jarduera-koefizientea
– Hidrogeno ioien kontzentrazioa
Jarduera-koefizientea ioien kontzentrazioaren funtzioa da eta 1era hurbiltzen da, disoluzioa gero eta gehiago diluitzen den heinean.
Disoluzio diluituetarako (idealetarako), solutuaren egoera estandarra 1,00 M da, beraz, bere molaritatea bere jarduera berdina da.
Beraz, soluzio idealak hartzen dituzten problema gehienetarako kontzentrazio molararen 10 oinarriaren logaritmoa erabil dezakegu, ez jarduera.
pH-aren eta pOH-ren balioaren arteko desberdintasunak

Zein da pH-aren balio normala?
- Nolabait esateko, pH hori neurri bat da disoluzio baten azidotasun edo alkalinitate maila ezartzeko erabiltzen da. "p"-ak "potentzial" esan nahi du, horregatik pH-a deitzen da: hidrogenoaren potentziala.
Zein da pOH balioa?
- Zure aldetik. pOH disoluzio batean hidroxilo ioien kontzentrazioa neurtzen da. Hidroxilo ioiaren kontzentrazioko 10 base logaritmo negatibo gisa adierazten da eta, pH-a ez bezala, disoluzio baten alkalinitate maila neurtzeko erabiltzen da.

Nola kalkulatzen da pH edo pOH balioa?
Zein da ph eskalaren balioen formula?
- Dagoeneko jakina denez, arlo zientifikoan, pH neurria da de barruko ioiak de irtenbide bat. Baliteke behar izatea kalkulatu pH-a kontzentrazioan oinarrituta. Kalkulatu pH ren ekuazioa erabiliz pH: pH = -log[H3O+].
Zein da pOH kalkulatzeko formula?
- Gainera, pOH (edo OH potentziala) disoluzio baten basikotasunaren edo alkalinitatearen neurria da. Gainera se pH = – log [H] erabiltzen du3O+] hidronio ioien kontzentrazioa neurtzeko [H3O+].

pH edo pOH balioa kalkulatzeko funtsezko ekuazioak
- pH=−log[H3O+]
- pOH=−log[OH−]
- [H3O+] = 10-pH
- [oh-] = 10-pOH
- pH + pOH =pKw = 14.00 25 °C-tan.
Zein da pH balioen eskalaren eta pOHaren arteko aldea?
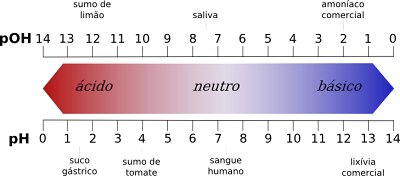
pH eskalaren balioen arteko desberdintasunak
- Alde batetik, pH eskalak 1etik 6rako azido-balioak ematen ditu, eta pOH eskalak 8-tik 14rako azido-balioak ematen ditu.
- Aitzitik, pH eskalak 8tik 14ra bitarteko oinarrizko balioak ematen ditu, eta pOH eskalak 1etik 6ra bitarteko oinarrizko balioak ematen ditu.
Ph-ren eta pOH-ren logaritmo-eskala erlazioa haien balioekin
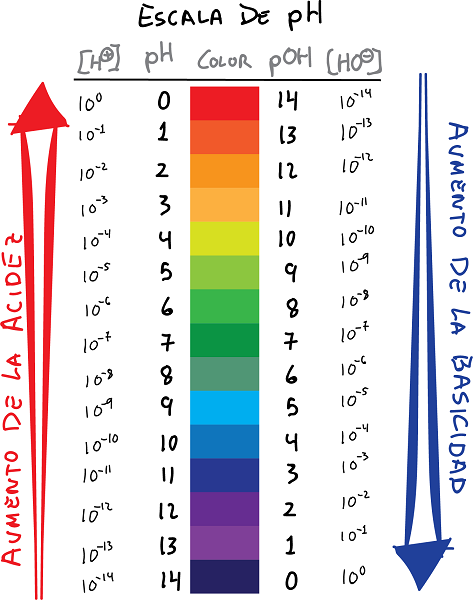
ph eta pOH eskalaren konexioa koloreekin eta balioekin
- pH H ioien kontzentrazioaren logaritmoa da+, zeinua aldatuta:
- Era berean, definitu pOH OH ioien kontzentrazioko logaritmo gisa-, zeinua aldatuta: ondoko erlazioa ezarri daiteke pH eta pOH.
- Funtsean, pH balioek hidrogeno ioiaren kontzentrazio logaritmo negatiboa ematen dute, eta pOH balioak hidroxido ioiaren kontzentrazio logaritmo negatiboa ematen du.
pH eta pOH balioen eskalaren arteko aldea
Ph balio-taularen eta pOH balioaren arteko desadostasunak
Horren ostean, pelikula bat eskaintzen dizugu non ikus dezakezun pH-ak hidrogeno ioien kontzentrazioa neurtzen duela, eta pOHk, berriz, hidroxilo anioien edo hidroxido ioien kontzentrazioa.


